

Siła skurczowa dowolnej długości jednostki na powierzchni cieczy nazywa się napięciem powierzchniowym, a jednostka jest N. · M-1.

Właściwość zmniejszania napięcia powierzchniowego rozpuszczalnika nazywa się aktywnością powierzchniową, a substancja o tej właściwości nazywa się substancją aktywną powierzchniową.
Substancja aktywna powierzchniowo, która może wiązać cząsteczki w roztworze wodnym i tworzyć micele i inne skojarzenia, a także mają wysoką aktywność powierzchniową, jednocześnie wpływającą na zwilżanie, emulgowanie, spienianie, mycie itp., Nazywa się środkiem powierzchniowo czynnym.
Surfaktant to związki organiczne o specjalnej strukturze i właściwości, które mogą znacząco zmienić napięcie międzyfazowe między dwiema fazami lub napięciem powierzchniowym cieczom (ogólnie wody), z zwilżaniem, pienim, emulgacją, myciem i innymi właściwościami.
Pod względem struktury środki powierzchniowo czynne mają wspólną cechę, ponieważ zawierają dwie grupy o różnych naturach w swoich cząsteczkach. Na jednym końcu znajduje się długi łańcuch grupy niepolarnej, rozpuszczalny w oleju i nierozpuszczalny w wodzie, znany również jako grupa hydrofobowa lub grupa odporna na wodę. Taka grupa wodna jest na ogół długimi łańcuchami węglowodorów, czasem również dla fluoru organicznego, krzemowego, organomofosforanu, łańcucha organotyny itp. Na drugim końcu znajduje się grupa rozpuszczalna w wodzie, grupa hydrofilowa lub grupa powtarzająca olej. Grupa hydrofilowa musi być wystarczająco hydrofilowa, aby upewnić się, że całe środki powierzchniowo czynne są rozpuszczalne w wodzie i mają niezbędną rozpuszczalność. Ponieważ środki powierzchniowo czynne zawierają grupy hydrofilowe i hydrofobowe, mogą być rozpuszczalne w co najmniej jednej fazie ciekłej. Ta hydrofilowa i lipofilowa właściwość środka powierzchniowo czynnego nazywana jest amfifilowością.


Surfaktant jest rodzajem cząsteczek amfifilowych z grupami hydrofobowymi, jak i hydrofilowymi. Grupy hydrofobowe środków powierzchniowo czynnych składają się na ogół z długotrwałego łańcucha węglowodorów, takich jak prosty łańcuch alkil C8 ~ C20, rozgałęziony alkil C8 ~ C20, alkilofenylu (liczba Tomu węglowego alkilowego wynosi 8 ~ 16) i podobne. Różnica, która jest niewielka między grupami hydrofobowymi, polega głównie na zmianach strukturalnych łańcuchów węglowodorów. A rodzaje grup hydrofilowych są większe, więc właściwości środków powierzchniowo czynnych są głównie związane z grupami hydrofilowymi oprócz wielkości i kształtu grup hydrofobowych. Zmiany strukturalne grup hydrofilowych są większe niż w grupach hydrofobowych, więc klasyfikacja środków powierzchniowo czynnych jest ogólnie oparta na strukturze grup hydrofilowych. Ta klasyfikacja opiera się na tym, czy grupa hydrofilowa jest jonowa, czy nie, i jest podzielona na anionowe, kationowe, niejonowe, ztolioniowe i inne specjalne typy środków powierzchniowo czynnych.

① Adsorpcja środków powierzchniowo czynnych na interfejsach
Cząsteczki środków powierzchniowo czynnych to cząsteczki amfifilowe o grupach lipofilowych i hydrofilowych. Gdy środek powierzchniowo czynny rozpuszczany jest w wodzie, jego hydrofilową grupę przyciąga wodę i rozpuszcza się w wodzie, podczas gdy jego lipofilowa grupa jest odpychana przez wodę i pozostawia wodę, co powoduje adsorpcję cząsteczek środków powierzchniowo czynnych (lub jonów) na interfejsie dwóch faz, co zmniejsza napięcie międzyfazowe między dwiema fazami. Im więcej cząsteczek środków powierzchniowo czynnych (lub jonów) jest adsorbowane na interfejsie, tym większe zmniejszenie napięcia międzyfazowego.
② Niektóre właściwości błony adsorpcji
Ciśnienie powierzchniowe membrany adsorpcji: adsorpcja środka powierzchniowo czynnego na interfejsie gazu-ciecz w celu utworzenia membrany adsorpcyjnej, takiej jak umieszczenie bez tarcia, zdejmowanego pływającego arkusza pływającego na interfejsie, pływające arkusz przesuwa membranę adsorbentową wzdłuż powierzchni roztworu, a błona generuje ciśnienie na pływowym arkuszu, które nazywane jest ciśnieniem powierzchni.
Lepkość powierzchni: podobnie jak ciśnienie powierzchniowe, lepkość powierzchni jest właściwością wykazującą nierozpuszczalną błonę molekularną. Zawieszony drobnym metalowym pierścieniem z drutu platynowego, tak że jego płaszczyzna styka się z powierzchnią wody zbiornika, obracaj pierścień platynowy, pierścień platynowy przez lepkość przeszkód wody, amplituda stopniowo rozkłada się, zgodnie z którym można zmierzyć lepkość powierzchni. Metoda jest następująca: Po pierwsze, eksperyment jest przeprowadzany na czystej powierzchni wody w celu pomiaru rozpadu amplitudy, a następnie mierzono rozkład po utworzeniu błony powierzchniowej, a lepkość błony powierzchniowej wynika z różnicy między nimi.
Lepkość powierzchni jest ściśle związana z solidnością błony powierzchniowej, a ponieważ membrana adsorpcyjna ma ciśnienie powierzchniowe i lepkość, musi mieć elastyczność. Im wyższe ciśnienie powierzchniowe i wyższa lepkość adsorbowanej membrany, tym wyższy moduł sprężysty. Moduł sprężystości membrany adsorpcji powierzchniowej jest ważny w procesie stabilizacji pęcherzyków.
③ Tworzenie miceli
Rozwodnione roztwory środków powierzchniowo czynnych przestrzegają przepisów, a następnie idealnych rozwiązań. Ilość środka powierzchniowo czynnego zaadsorbowanego na powierzchni roztworu wzrasta wraz ze stężeniem roztworu, a gdy stężenie osiąga lub przekracza określoną wartość, ilość adsorpcji nie wzrasta, a te nadmiar cząsteczek surfaktantów znajdują się w roztworze w sposób przypadkowy lub w sposób regularny. Zarówno praktyka, jak i teoria pokazują, że tworzą skojarzenia w rozwiązaniu, a skojarzenia te nazywane są micele.
Krytyczne stężenie miceli (CMC): Minimalne stężenie, przy którym środki powierzchniowo czynne tworzą micele w roztworze, nazywa się krytycznym stężeniem miceli.
④ Wartości CMC wspólnych środków powierzchniowo czynnych.

HLB jest skrótem hydrofilowego bilansu lipofilowego, co wskazuje na hydrofilową i lipofilową równowagę hydrofilowych i lipofilowych grup środka powierzchniowo czynnego, tj. Wartość HLB środka powierzchniowo czynnego. Duża wartość HLB wskazuje na cząsteczkę o silnej hydrofilowości i słabej lipofilności; I odwrotnie, silna lipofilność i słaba hydrofilowość.
① Postanowienia wartości HLB
Wartość HLB jest wartością względną, więc gdy wartość HLB jest opracowana, jako standard, wartość HLB wosku parafinowego, który nie ma właściwości hydrofilowych, jest określana jako 0, podczas gdy wartość HLB od 1 do 40. Ogólnie rzecz biorąc, emulgatów, która jest bardziej rozpuszczalna w ilości wody niż o rozpuszczaniu wody niż rozpuszczalna w wodzie, jest mniej rozpuszczalna w wodzie. 10 są lipofilowe, podczas gdy ponad 10 są hydrofilowe. Zatem punkt zwrotny od lipofilowy do hydrofilowy wynosi około 10.
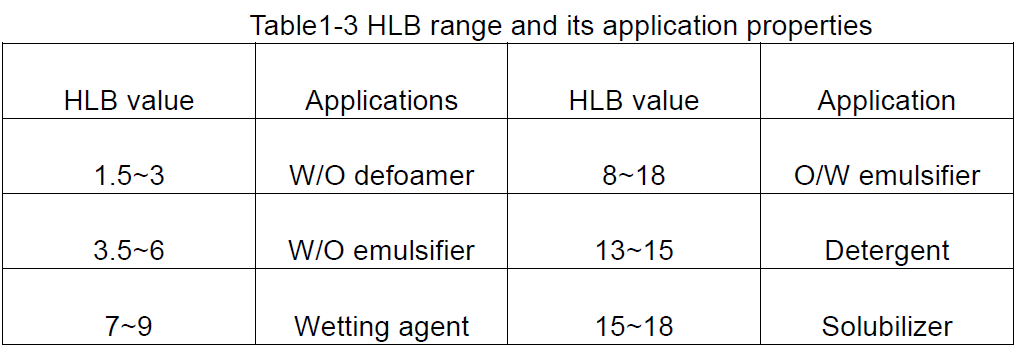
Na podstawie wartości HLB środków powierzchniowo czynnych można uzyskać ogólną ideę ich możliwych zastosowań, jak pokazano w tabeli 1-3.

Dwie wzajemnie nierozpuszczalne ciecze, jedna rozproszona w drugiej jako cząstki (krople lub ciekłe kryształy) tworzą układ zwany emulsją. System ten jest niestabilny termodynamicznie ze względu na wzrost powierzchni granicznej dwóch cieczy po utworzeniu emulsji. Aby uczynić stabilną emulsję, konieczne jest dodanie trzeciego elementu - emulgatora w celu zmniejszenia energii międzyfazowej systemu. Emulgator należy do środka powierzchniowo czynnego, jego główną funkcją jest odgrywanie roli emulsji. Faza emulsji, która występuje jako kropelki, nazywa się fazą zdyspergowaną (lub fazą wewnętrzną, fazą nieciągłową), a druga połączona faza jest nazywana pożywką dyspergującą (lub fazą zewnętrzną, fazą ciągłą).
① emulgatory i emulsje
Wspólne emulsje, jedna faza to woda lub roztwór wodny, druga faza to substancje organiczne, które nie są mieszane z wodą, takimi jak tłuszcz, wosk itp. Emulsja utworzona przez wodę i olej można podzielić na dwa typy według ich sytuacji dyspersyjnej: olej rozproszony w wodzie z emulsją typu oleju w wodzie, wyrażoną jako O/W (olej/wodę): wodoodporne w celu wytworzenia oleju w wodę w wodę, w celu wytworzenia emulsji typu m-woda, A jak M w/O. (woda/olej). Można również utworzyć również złożoną wodę w oleju w wodzie w/O/W i olej-wodzie w oleju oleju.
Emulgatory stosuje się do stabilizacji emulsji poprzez zmniejszenie napięcia międzyfazowego i utworzenie membrany międzyfazowej pojedynczej cząsteczki.
W emulgowaniu wymagań emulgatora:
Odp.: emulgator musi być w stanie adsorbować lub wzbogacić interfejs między dwiema fazami, tak że napięcie międzyfazowe zostało zmniejszone;
B: emulgator musi nadać cząsteczki ładunku, aby elektrostatyczne odpychanie między cząsteczkami lub tworzy stabilną, wysoce lepką błonę ochronną wokół cząstek.
Dlatego substancja stosowana jako emulgator musi mieć grupy amfifilowe w celu emulgowania, a środki powierzchniowo czynne mogą spełniać ten wymóg.
② Metody przygotowania emulsji i czynników wpływających na stabilność emulsji
Istnieją dwa sposoby przygotowania emulsji: jeden jest zastosowanie metody mechanicznej w celu rozproszenia cieczy w maleńkich cząstkach w innej cieczy, która jest najczęściej stosowana w przemyśle do przygotowania emulsji; Drugim jest rozpuszczenie cieczy w stanie molekularnym w innej cieczy, a następnie prawidłowo gromadzenie się, aby utworzyć emulsje.
Stabilność emulsji polega na zdolności do agregacji przeciwdziałowej, która prowadzi do rozdziału faz. Emulsje to systemy niestabilne termodynamicznie o dużej energii swobodnej. Dlatego tak zwana stabilność emulsji jest w rzeczywistości czasem wymaganym do osiągnięcia równowagi, tj. Czas wymagany do oddzielenia jednej cieczy w układzie.
Gdy błona międzyfazowa z alkoholem tłuszczowym, kwasami tłuszczowymi i aminami tłuszczowymi oraz innymi polarnymi cząsteczkami organicznymi, wytrzymałość błony znacznie wyższa. Wynika to z faktu, że w międzyfazowej warstwie adsorpcji cząsteczek i alkoholi emulgatora, kwasów i amin oraz innych cząsteczek polarnych tworząc „złożone”, tak że zwiększona wytrzymałość błony międzyfazowej.
Emulgatory składające się z więcej niż dwóch środków powierzchniowo czynnych nazywane są mieszanymi emulgatorami. Mieszany emulgator zaadsorbowany na interfejsie wody/oleju; Działanie międzycząsteczkowe może tworzyć kompleksy. Ze względu na silne działanie międzycząsteczkowe napięcie międzyfazowe jest znacznie zmniejszone, ilość emulgatora zaadsorbowanego na interfejsie jest znacznie zwiększona, powstawanie gęstości błony międzyfazowej wzrasta wytrzymałość.
Ładunek cieczy perełek ma znaczący wpływ na stabilność emulsji. Stabilne emulsje, których ciekłe koraliki są ogólnie naładowane. Gdy stosuje się emulgator jonowy, jon emulsyjny zaadsorbowany na interfejsie ma swoją lipofilową grupę wkładaną do fazy olejowej, a grupa hydrofilowa znajduje się w fazie wodnej, co powoduje naładowane ciekłe kulki. Jako koraliki emulsji o tym samym ładunku, odpychają się nawzajem, nie są łatwe do aglomeratu, tak że stabilność została zwiększona. Można zauważyć, że im więcej jonów emulgatora zaadsorbowane na koralikach, tym większa ładunek, tym większa zdolność do zapobiegania aglomeracji koralików, tym bardziej stabilny układ emulsji.
Lepkość podłoża dyspersji emulsji ma pewien wpływ na stabilność emulsji. Zasadniczo im wyższa lepkość podłoża dyspersji, tym wyższa stabilność emulsji. Wynika to z faktu, że lepkość ośrodka dyspersji jest duża, co ma silny wpływ na ruch brązu cieczy i spowalnia kolizję między ciekłymi koralikami, dzięki czemu system pozostał stabilny. Zwykle substancje polimerowe, które można rozpuścić w emulsjach, mogą zwiększyć lepkość układu i zwiększyć stabilność emulsji. Ponadto polimery mogą również tworzyć silną błonę międzyfazową, dzięki czemu układ emulsji jest bardziej stabilny.
W niektórych przypadkach dodanie stałego proszku może również sprawić, że emulsja ma tendencję do stabilizacji. Stały proszek znajduje się w wodzie, oleju lub interfejsie, w zależności od oleju, woda na motowaniu stałego proszku, jeśli stały proszek nie jest całkowicie mokry z wodą, ale także mokry przez olej, pozostanie na interfejsie wody i oleju.
Stały proszek nie sprawia, że emulsja jest stabilna, ponieważ proszek zebrany na interfejsie wzmacnia błonę międzyfazową, która jest podobna do międzyfazowej adsorpcji cząsteczek emulgatora, więc im bardziej stały materiał proszku jest rozmieszczony na interfejsie, tym bardziej stabilny jest emulsja.
Surfaktanty mają zdolność znacznego zwiększenia rozpuszczalności nierozpuszczalnych lub lekko rozpuszczalnych w wodzie substancji organicznych po utworzeniu miceli w roztworze wodnym, a roztwór jest w tym czasie przezroczysty. Ten efekt miceli nazywa się rozpuszczeniem. Surfaktant, który może powodować rozpuszczenie, nazywa się rozpuszczeniem, a materia organiczna, która jest rozpuszczona, nazywa się materią solubilizowaną.

Piana odgrywa ważną rolę w procesie mycia. Piana jest układem dyspersyjnym, w którym gaz jest rozproszony w cieczy lub substancji stałej, z gazem jako rozproszoną fazą i cieczy lub stałą jako podłoże rozpraszającego, a pierwsza nazywana jest pianką ciekłą, podczas gdy druga nazywa się pianką stałą, taką jak spieniona plastik, pienista, spieniona cement, cement itp.
(1) Tworzenie pianki
Przez piankę rozumiemy tutaj kruszyw pęcherzyków powietrza oddzielonych płynną błoną. Ten rodzaj pęcherzyka zawsze wznosi się szybko do powierzchni cieczy z powodu dużej różnicy gęstości między fazą dyspergowaną (gazem) a pożywką dyspergującą (ciecz), w połączeniu z niską lepkością cieczy.
Proces tworzenia bańki polega na wprowadzeniu dużej ilości gazu do cieczy, a pęcherzyki w cieczy szybko wracają na powierzchnię, tworząc agregat pęcherzyków oddzielonych niewielką ilością gazu ciekłego.
Piana ma dwie istotne cechy pod względem morfologii: jeden jest taki, że pęcherzyki jako rozproszonej fazy mają często wielościennikowy kształt, dzieje się tak, ponieważ na przecięciu bąbelków istnieje tendencja do cienkiej folii, tak aby pęcherzyki stały się wielościenne, gdy ciekła folia Thins Thins do pewnego odległości, prowadzi do pęknięcia; Po drugie, czyste ciecze nie mogą tworzyć stabilnej pianki, ciecz, która może tworzyć piankę, wynosi co najmniej dwa lub więcej elementów. Wodne roztwory środków powierzchniowo czynnych są typowe dla systemów podatnych na wytwarzanie pianki, a ich zdolność do generowania pianki jest również związana z innymi właściwościami.
Środki powierzchniowo czynne o dobrej mocy pieniaka nazywane są środkami pieniącymi. Chociaż środek pieniący ma dobrą zdolność pianki, ale utworzona piana może nie być w stanie utrzymać długo, to znaczy jego stabilność niekoniecznie jest dobra. Aby utrzymać stabilność pianki, często w środku pieniącym się w celu dodania substancji, które mogą zwiększyć stabilność pianki, substancja nazywa się stabilizatorem pianki, powszechnie stosowanym stabilizatorem jest dietanoloamina laurylowa i tlenek dodecylu dimetyloaminy.
(2) Stabilność pianki
Piana jest systemem niestabilnym termodynamicznie, a końcowym trendem jest to, że całkowity powierzchnia cieczy w układzie maleje po zerwaniu bańki, a energia swobodna maleje. Proces defoamowania to proces, w którym płynna membrana oddzielająca gaz staje się grubszy i cieńszy, aż się pęknie. Dlatego stopień stabilności pianki wynika głównie z prędkości wyładowania ciekłego i wytrzymałością folii ciekłej. Wpływają na to również następujące czynniki.
(3) Zniszczenie pianki
Podstawową zasadą zniszczenia pianki jest zmiana warunków wytwarzających pianę lub wyeliminowanie czynników stabilizujących pianki, dlatego istnieją zarówno fizyczne, jak i chemiczne metody defoaming.
Fizyczne defoamowanie oznacza zmianę warunków produkcji pianki przy jednoczesnym utrzymaniu składu chemicznego roztworu piankowego, takiego jak zaburzenia zewnętrzne, zmiany temperatury lub ciśnienia i obróbka ultradźwiękowa są skutecznymi fizycznymi metodami eliminowania pianki.
Metodą defoamowania chemicznego polega na dodaniu niektórych substancji do interakcji z środkiem pieniącym w celu zmniejszenia wytrzymałości filmu ciekłego w piance, a tym samym zmniejszeniem stabilności pianki w celu osiągnięcia celu defoamowania, takie substancje nazywane są defoamery. Większość defoamerów to środki powierzchniowo czynne. Dlatego, zgodnie z mechanizmem defoamingu, defoamer powinien mieć silną zdolność do zmniejszania napięcia powierzchniowego, łatwego do adsorbowania na powierzchni, a interakcja między cząsteczkami adsorpcji powierzchniowej jest słabe, cząsteczki adsorpcji ułożone w bardziej rozluźną strukturę.
Istnieją różne rodzaje defoamerów, ale w zasadzie wszystkie są niejonowymi środkami powierzchniowo czynnymi. Środkowe czynniki powierzchniowo czynne mają właściwości przeciwdziałające foamie w pobliżu lub powyżej ich punktu chmur i są często używane jako defoamery. Alkohole, zwłaszcza alkohole o rozgałęzionej strukturze, kwasach tłuszczowych i estrach kwasów tłuszczowych, poliamidy, estry fosforanowe, oleje silikonowe itp. Są również powszechnie stosowane jako doskonałe defoamery.
(4) Piana i mycie
Nie ma bezpośredniego związku między pianką a skutecznością prania, a ilość piany nie wskazuje na skuteczność prania. Na przykład niejonowe środki powierzchniowo czynne mają znacznie mniej właściwości spędzonych niż mydła, ale ich odkażanie jest znacznie lepsze niż mydła.
W niektórych przypadkach piana może być pomocna w usuwaniu brudu i brudu. Na przykład, gdy myje naczynia w domu, piana detergentu podnosi kropelki oleju, a podczas szorowania dywanów pianka pomaga zebrać kurz, proszek i inne solidne brud. Ponadto piankę można czasem stosować jako wskazanie skuteczności detergentu. Ponieważ oleje tłuszczowe mają wpływ hamujący na piankę detergentu, gdy jest zbyt dużo oleju i za mało detergentu, nie będzie wytworzona pianka lub oryginalna piana zniknie. Pianę może być czasem używana jako wskaźnik czystości płukania, ponieważ ilość piany w roztworze płukania ma tendencję do zmniejszania się wraz ze zmniejszeniem detergentu, więc ilość piany można zastosować do oceny stopnia płukania.
W szerokim sensie mycie jest procesem usuwania niechcianych komponentów z obiektu, które mają być umyte i osiągnąć jakiś cel. Mycie w zwykłym sensie odnosi się do procesu usuwania brudu z powierzchni nośnika. Podczas mycia interakcja między brukiem a nośnikiem jest osłabiona lub eliminowana przez działanie niektórych substancji chemicznych (np. Detergent itp.), Tak aby połączenie brudu i nośnika zmieniło się w kombinację brudu i detergentu, a wreszcie brud jest oddzielony od nośnika. Ponieważ obiekty, które należy umyć, a brud do usunięcia jest zróżnicowany, mycie jest bardzo złożonym procesem, a podstawowy proces mycia można wyrazić w następujących prostych związkach.
Carrie ·· Dirt + detergent = nośnik + detergent · detergent
Proces mycia można zwykle podzielić na dwa etapy: po pierwsze, pod działaniem detergentu, brud jest oddzielony od jego przewoźnika; Po drugie, oderwany brud jest rozproszony i zawieszony w medium. Proces mycia jest procesem odwracalnym, a brud rozproszony i zawieszony w medium może być również ponownie precypitowany od środka do mycia obiektu. Dlatego dobry detergent powinien mieć możliwość rozproszenia i zawieszenia brudu oraz zapobiegania ponownym wydawaniu brudu, oprócz możliwości usuwania brudu z nośnika.
(1) Rodzaje brudu
Nawet w przypadku tego samego elementu typ, skład i ilość brudu mogą się różnić w zależności od środowiska, w którym jest używany. Brud w ciele oleju to głównie niektóre oleje ze zwierząt i roślinnych oraz oleje mineralne (takie jak ropa naftowa, olej opałowy, smoła węglowa itp.), Brud stały jest głównie sadzy, popiołu, rdzy, sadzy itp. Jeśli chodzi o odzież, jest brud z ciała ludzkiego, takie jak pot, sebum, krew itp. Brud z jedzenia, taki jak plamy owocowe, plamy oleju kuchennego, plamy przypraw, skrobia itp.; Drug z kosmetyków, taki jak szminka, lakier do paznokci itp.; brud z atmosfery, taki jak sadza, kurz, błoto itp.; Inne, takie jak atrament, herbata, powłoka itp. Występuje w różnych typach.
Różne rodzaje brudu można zwykle podzielić na trzy główne kategorie: solidny brud, brud i brud specjalny.
① Solidny brud
Wspólny stały brud obejmuje cząstki popiołu, błota, ziemi, rdzy i sadzy. Większość z tych cząstek ma ładunek elektryczny na swojej powierzchni, większość z nich jest ujemnie naładowana i może być łatwo adsorbowana na elementach włókien. Brud stały jest ogólnie trudny do rozpuszczenia w wodzie, ale można go rozproszyć i zawieszać przez roztwory detergentowe. Solidny brud z mniejszym punktem masowym jest trudniejszy do usunięcia.
② Płynny brud
Płynny brud jest w większości rozpuszczalny w oleju, w tym oleje roślinne i zwierzęce, kwasy tłuszczowe, alkohole tłuszczowe, oleje mineralne i ich tlenki. Wśród nich mogą wystąpić oleje roślinne i zwierzęce, kwasy tłuszczowe i saponifikacja alkaliczna, podczas gdy alkohole tłuszczowe, oleje mineralne nie są saponifikowane przez alkaliczne, ale mogą być rozpuszczalne w alkoholi, eterach i rozpuszczalnikach organicznych węglowodorów oraz emulgowaniu i rozpuszczaniu roztworu wodnego detergentu. Rozpuszczalny w oleju brud ma na ogół silną siłę z elementami włókien i jest mocniej adsorbowany na włóknach.
③ Specjalny brud
Specjalny brud obejmuje białka, skrobię, krew, ludzkie wydzieliny, takie jak pot, sebum, sok z moczu i owoców oraz sok z herbaty. Większość tego rodzaju brudu może być chemicznie i silnie adsorbowana na elementach błonnika. Dlatego trudno jest umyć.
Różne rodzaje brudu są rzadko spotykane same, ale często są mieszane razem i adsorbowane na obiekcie. Brud można czasem utleniać, rozłożyć lub rozkładać pod wpływami zewnętrznymi, tworząc w ten sposób nowy brud.
(2) Przyczepność brudu
Ubrania, ręce itp. Można zabarwić, ponieważ istnieje jakaś interakcja między przedmiotem a brudem. Brud przylega do przedmiotów na różne sposoby, ale nie ma więcej niż fizyczne i chemiczne zrosty.
① Przyczepność sadzy, kurzu, błota, piasku i węgla drzewnego do odzieży jest przyczepnością fizyczną. Ogólnie rzecz biorąc, poprzez tę przyczepność brudu, a rola między zabarwionym obiektem jest stosunkowo słaba, usuwanie brudu jest również stosunkowo łatwe. Według różnych sił fizyczna przyczepność brudu można podzielić na mechaniczną przyczepność i adhezję elektrostatyczną.
Odp.: Przyczepność mechaniczna
Ten rodzaj przyczepności odnosi się głównie do przyczepności jakiegoś stałego brudu (np. Pył, błota i piasku). Adhezja mechaniczna jest jedną ze słabszych form przyczepności brudu i można ją usunąć prawie czysto mechanicznymi środkami, ale gdy brud jest niewielki (<0,1um), trudniej jest go usunąć.
B : Przyczepność elektrostatyczna
Adhezja elektrostatyczna objawia się głównie w działaniu naładowanych cząstek polnych na przeciwnie naładowanych obiektach. Większość włóknistych obiektów jest ujemnie naładowana w wodzie i może być łatwo przestrzegana przez niektóre pozytywnie naładowane brud, takie jak typy wapna. Niektóre brud, choć ujemnie naładowane, takie jak cząsteczki sadzy w roztworach wodnych, mogą przylegać do włókien przez mosty jonowe (jony między wieloma przeciwnie naładowanymi obiektami, działając wraz z nimi w sposób podobny do mostu) utworzone przez jony dodatnie w wodzie (np. Ca2+, mg2+ itp.).
Działanie elektrostatyczne jest silniejsze niż proste działanie mechaniczne, co utrudnia usuwanie brudu.
② Przyczepność chemiczna
Adhezja chemiczna odnosi się do zjawiska brudu, działającego na obiekt poprzez wiązania chemiczne lub wodorowe. Na przykład polarne stałe brud, białko, rdza i inne przyczepność na elementach błonnika, włókna zawierają karboksyl, hydroksyl, amid i inne grupy, te grupy i tłuste kwasy tłuszczowe, alkohole tłuszczowe są łatwe do wytworzenia wiązań wodorowych. Siły chemiczne są na ogół silne, a zatem brud jest mocniej związany z obiektem. Ten rodzaj brudu jest trudny do usunięcia zwykłymi metodami i wymaga specjalnych metod, aby sobie z tym poradzić.
Stopień przyczepności brudu jest związany z naturą samego brudu i naturą obiektu, do którego jest przestrzegany. Zasadniczo cząstki łatwo przylegają do elementów włóknistych. Im mniejsza tekstura solidnego brudu, tym silniejsza przyczepność. Polarne brud na obiektach hydrofilowych, takich jak bawełna i szkło, są silniejsze niż brud niepolarny. Niepolarne brud przylewa się silniej niż brud polarny, taki jak tłuszcze polarne, kurz i glina, i jest mniej łatwa do usunięcia i czyszczenia.
(3) Mechanizm usuwania brudu
Celem mycia jest usuwanie brudu. W medium o określonej temperaturze (głównie wodzie). Wykorzystując różne fizyczne i chemiczne działanie detergentu w celu osłabienia lub wyeliminowania efektu brudu i przemytych obiektów, pod działaniem niektórych sił mechanicznych (takich jak pocieranie ręki, mieszanie pralki, uderzenie wody), tak że brudz i obiekty z celu odkażania.
① Mechanizm usuwania brud płynnych
A : Nocz
Płynne zabrudzenie jest głównie na bazie oleju. Plamy olejowe mokre najbardziej włókniste przedmioty i rozprzestrzeniają się mniej więcej jako warstwę oleju na powierzchni włóknistego materiału. Pierwszym krokiem w działaniu mycia jest zwilżanie powierzchni przez płyn prania. Ze względu na ilustrację powierzchnię włókna można traktować jako gładką stałą powierzchnię.
B: Odłączanie oleju - mechanizm zwijania
Drugim krokiem w myciu jest usuwanie oleju i tłuszczu, usuwanie płynnego brudu osiąga się przez rodzaj zwinięcia. Pierwotnie brud płynny istniał na powierzchni w postaci rozprzestrzeniania się folii olejowej i pod preferencyjnym efektem zwilżania cieczy myjącej na stałej powierzchni (tj., Powierzchni włókien), skręcał się w kulki olejowej krok po kroku, które zostały zastąpione płyną prania i ostatecznie opuścił powierzchnię pod pewnymi siłami zewnętrznymi.
② Mechanizm usuwania stałego brudu
Usunięcie ciekłego brudu odbywa się głównie przez preferencyjne zwilżanie nośnika brudu przez roztwór mycia, podczas gdy mechanizm usuwania stałego brudu jest inny, gdzie proces mycia dotyczy głównie zwilżania masy brudu i jej powierzchni nośnej przez roztwór mycia. Ze względu na adsorpcję środków powierzchniowo czynnych na stałym bruku i jego powierzchni nośnej interakcja między brudem a powierzchnią jest zmniejszona, a wytrzymałość na adhezję masy brudu na powierzchni jest zmniejszona, dlatego masa brudu jest łatwo usuwana z powierzchni nośnika.
Ponadto adsorpcja środków powierzchniowo czynnych, zwłaszcza jonowych środków powierzchniowo czynnych, na powierzchni stałego brudu i jego nośnika może potencjalnie zwiększyć potencjał powierzchniowy na powierzchni stałego brudu i jego nośnika, który bardziej sprzyjający usuwaniu brudu. Solidne lub ogólnie włókniste powierzchnie są zwykle ujemnie naładowane w pożywce wodnej, a zatem mogą tworzyć rozproszone podwójne warstwy elektroniczne na masach polnych lub powierzchniach stałych. Z powodu odpychania jednorodnych ładunków osłabia się przyczepność cząstek polnych w wodzie na stałą powierzchnię. Gdy dodaje się anionowy środek powierzchniowo czynny, ponieważ może jednocześnie zwiększyć ujemny potencjał powierzchniowy cząstki polnej i powierzchni stałej, odpychanie między nimi jest bardziej zwiększone, wytrzymałość adhezji cząstki jest bardziej zmniejszona, a brudu jest łatwiejszy do usunięcia.
Niejoniczne środki powierzchniowo czynne są adsorbowane na ogólnie naładowanych powierzchniach stałych i chociaż nie zmieniają znacząco potencjału międzyfazowego, zaadsorbowane niejonowe środki powierzchniowo czynne mają tendencję do tworzenia pewnej grubości zaadsorbowanej warstwy na powierzchni, która pomaga zapobiec ponownemu nadpozycji brudu.
W przypadku kationowych środków powierzchniowo czynnych ich adsorpcja zmniejsza lub eliminuje ujemny potencjał powierzchniowy masy brudu i jej powierzchni nośnika, co zmniejsza odpychanie między brukiem a powierzchnią i dlatego nie sprzyjają usuwaniu brudu; Ponadto, po adsorpcji na powierzchni stałej, kationowe środki powierzchniowo czynne mają tendencję do obracania stałej powierzchni hydrofobowej i dlatego nie sprzyjają zwilżaniu powierzchni, a zatem mycie.
③ Usunięcie specjalnych gleb
Białko, skrobia, wydzieliny ludzkie, sok owocowy, sok z herbaty i inne takie brud są trudne do usunięcia z normalnymi środkami powierzchniowo czynnymi i wymagają specjalnego leczenia.
Plamy białkowe, takie jak krem, jaja, krew, mleko i wydatki skóry, mają tendencję do koagulacji na włóknach i degeneracji oraz silniejszej przyczepności. Zabrudzenie białka można usunąć za pomocą proteaz. Proteaza enzymatyczna rozkłada białka w brudzie na rozpuszczalne w wodzie aminokwasy lub oligopeptydy.
Plamy skrobiowe pochodzą głównie z produktów spożywczych, inne, takie jak sos, klej itp. Amylaza ma katalityczny wpływ na hydrolizę plam skrobi, powodując rozpadnięcie skrobi na cukry.
Lipaza katalizuje rozkład trójglicerydów, które są trudne do usunięcia normalnymi metodami, takimi jak sebum i oleje jadalne, i rozkładają je na rozpuszczalne glicerolu i kwasy tłuszczowe.
Niektóre kolorowe plamy z soków owocowych, soków herbacianych, atramentów, szminki itp. Są często trudne do dokładnego wyczyszczenia nawet po wielokrotnym myciu. Plamy te można usunąć przez reakcję redoks z środkiem utleniającym lub redukującym, takim jak wybielacz, który niszczy strukturę grup generujących kolor lub kolor kolorów i degraduje je w mniejsze elementy rozpuszczalne w wodzie.
(4) Mechanizm usuwania plam plamy
Powyższe jest właściwie dla wody jako środka mycia. W rzeczywistości, ze względu na różne rodzaje odzieży i struktury, niektóre ubrania za pomocą mycia wody nie są wygodne lub nie są łatwe do umycia, niektóre odzież po umyciu, a nawet deformacji, blaknięciu itp., Na przykład: większość naturalnych włókien pochłania wodę i łatwa do puchania, a sucha i łatwa do skurczania, więc po umyciu zostanie zdeformowana; Przez pranie produktów wełny często wydają się zjawiskiem skurczania, niektóre wełniane produkty z myciem wody są również łatwe do wypoczynku, zmiana koloru; Niektóre jedwabie po umyciu stają się coraz gorsze po umyciu i utraty połysku. Do tych ubrań często używają metody czyszczenia na sucho do odkażania. Tak zwane czyszczenie na sucho ogólnie odnosi się do metody mycia w rozpuszczalnikach organicznych, szczególnie w rozpuszczalnikach niepolarnych.
Czyszczenie na sucho jest łagodniejszą postacią mycia niż mycie wody. Ponieważ czyszczenie na sucho nie wymaga dużego działania mechanicznego, nie powoduje uszkodzeń, marszczenia i deformacji odzieży, podczas gdy środki czyszczące na sucho, w przeciwieństwie do wody, rzadko wytwarzają ekspansję i skurcz. Dopóki technologia jest odpowiednio obsługiwana, ubrania można na sucho czyszczyć bez zniekształceń, zanikania kolorów i długotrwałej żywotności serwisowej.
Jeśli chodzi o czyszczenie na sucho, istnieją trzy szerokie rodzaje brudu.
Brud rozpuszczalny w rozpuszczalnym oleju, rozpuszczalny w oilliczach, obejmuje wszystkie rodzaje oleju i smaru, który jest płynny lub tłusty i może być rozpuszczony w rozpuszczalnikach na sucho czyszczącym.
② Rozpuszczalny w wód brudu rozpuszczalny w wodzie brud jest rozpuszczalny w roztworach wodnych, ale nie w środkach czyszczących na sucho, jest adsorbowany na odzieży w stanie wodnym, woda odparowuje po wytrącaniu ziarnistej substancji stałych, takich jak sole nieorganiczne, skrobia, białko itp.
Nie rozpuszczalny brud i woda nierozpuszczalna brud nie jest ani rozpuszczalny w wodzie, ani rozpuszczalny w rozpuszczalnikach o czyszczeniu na sucho, takim jak sadowa czarna, krzemiany różnych metali i tlenków itp.
Ze względu na różny charakter różnych rodzajów brudu istnieją różne sposoby usuwania brudu w procesie oczyszczania suchego. Gleby rozpuszczalne w oleju, takie jak oleje zwierzęce i roślinne, oleje mineralne i smarowe, są łatwo rozpuszczalne w rozpuszczalnikach organicznych i można je łatwiej usunąć podczas czyszczenia na sucho. Doskonała rozpuszczalność rozpuszczalników oczyszczających na sucho dla olejków i smarów zasadniczo pochodzi z sił ścian van der między cząsteczkami.
W celu usunięcia rozpuszczalnego w wodzie brudu, takich jak sole nieorganiczne, cukry, białka i pot, odpowiednią ilość wody należy również dodać do środka oczyszczającego suche, w przeciwnym razie trudne jest rozpuszczalne w wodzie brudu z odzieży. Jednak woda jest trudna do rozpuszczenia w środku oczyszczającym suchość, więc aby zwiększyć ilość wody, musisz również dodać środki powierzchniowo czynne. Obecność wody w środku oczyszczającym suchą może spowodować nawodnienie powierzchni brudu i odzieży, dzięki czemu łatwo jest oddziaływać z grupami polarnymi środków powierzchniowo czynnych, co sprzyja adsorpcji środków powierzchniowo czynnych na powierzchni. Ponadto, gdy środki powierzchniowo czynne tworzą micele, rozpuszczalny w wodzie brud i woda mogą być rozpuszczone do miceli. Oprócz zwiększenia zawartości wody w rozpuszczalniku do czyszczenia suchego, środki powierzchniowo czynne mogą również odgrywać rolę w zapobieganiu ponownym złożeniu brudu w celu zwiększenia efektu odkażania.
Obecność niewielkiej ilości wody jest niezbędna do usunięcia rozpuszczalnego w wodzie brudu, ale zbyt duża ilość wody może powodować zniekształcenie i zmarszczki w niektórych ubraniach, więc ilość wody w środku oczyszczającym suchość musi być umiarkowana.
Brud, który nie jest ani rozpuszczalny w wodzie, ani rozpuszczalny w oleju, cząsteczki stałe, takie jak popiół, błoto, ziemia i sadowa czarna, jest ogólnie przywiązana do odzieży przez siły elektrostatyczne lub w połączeniu z olejem. Podczas czyszczenia na sucho przepływ rozpuszczalnika uderzenie może spowodować, że adsorpcja siły elektrostatycznej zabrudzenia wyłączona, a środek czyszczenia suchego może rozpuścić olej, tak aby połączenie oleju i brudu i przymocowane do odzieży stałych cząstek w środku suchej czyszczącej, środka czyszczenia suchego w niewielkiej ilości wody i środków powierzchniowo czynnych, tak aby te nieobecne cząsteczki mogą być stałym zawieszeniem, dyspersji, aby zapobiec jego przełomowi w niewielkiej ilości wody i środków powierzchniowo czynnych, aby nie było rozpowszechniania. odzież.
(5) Czynniki wpływające na działanie mycia
Kierunkowa adsorpcja środków powierzchniowo czynnych na interfejsie i zmniejszenie napięcia powierzchniowego (międzyfazowego) są głównymi czynnikami w usuwaniu cieczy lub stałego brudu. Jednak proces mycia jest złożony, a na efekt mycia, nawet przy tym samym typie detergentu, wpływa wiele innych czynników. Czynniki te obejmują stężenie detergentu, temperaturę, charakter zabrudzenia, rodzaj błonnika i strukturę tkaniny.
① Stężenie środków powierzchniowo czynnych
Micele środków powierzchniowo czynnych w roztworze odgrywają ważną rolę w procesie mycia. Gdy stężenie osiąga krytyczne stężenie miceli (CMC), efekt mycia gwałtownie wzrasta. Dlatego stężenie detergentu w rozpuszczalniku powinno być wyższe niż wartość CMC, aby mieć dobry efekt mycia. Jednak gdy stężenie środka powierzchniowo czynnego jest wyższe niż wartość CMC, przyrostowy wzrost efektu mycia nie jest oczywisty i nie jest konieczne zbyt duże zwiększenie stężenia środka powierzchniowo czynnego.
Podczas usuwania oleju przez solubilizację efekt solubilizacji wzrasta wraz ze wzrostem stężenia środków powierzchniowo czynnych, nawet gdy stężenie jest powyżej CMC. W tej chwili wskazane jest używanie detergentu w sposób lokalny scentralizowany. Na przykład, jeśli na mankietach i kołnierzu jest dużo brudu, można zastosować warstwę detergentu podczas mycia, aby zwiększyć rozpuszczający wpływ środka powierzchniowo czynnego na olej.
②Temperature ma bardzo ważny wpływ na działanie odkażania. Zasadniczo zwiększenie temperatury ułatwia usuwanie brudu, ale czasem zbyt wysoka temperatura może również powodować wady.
Wzrost temperatury ułatwia dyfuzję brudu, tłuszcz stałego jest łatwo zemulgowany w temperaturach powyżej jego temperatury topnienia, a włókna rosną w obrzęku ze względu na wzrost temperatury, z których wszystkie ułatwiają usuwanie brudu. Jednak w przypadku kompaktowych tkanin mikrogapy między włóknami są zmniejszone w miarę rozszerzania się włókien, co jest szkodliwe dla usuwania brudu.
Zmiany temperatury wpływają również na rozpuszczalność, wartość CMC i wielkość miceli środków powierzchniowo czynnych, wpływając w ten sposób na efekt mycia. Rozpuszczalność środków powierzchniowo czynnych o długich łańcuchach węgla jest niska w niskich temperaturach, a czasem rozpuszczalność jest nawet niższa niż wartość CMC, więc temperatura mycia należy odpowiednio podnieść. Wpływ temperatury na wartość CMC i wielkość miceli jest inny dla jonowych i niejonowych środków powierzchniowo czynnych. W przypadku jonowych środków powierzchniowo czynnych wzrost temperatury ogólnie zwiększa wartość CMC i zmniejsza wielkość miceli, co oznacza, że należy zwiększyć stężenie środka powierzchniowo czynnego w roztworze mycia. W przypadku niejonowych środków powierzchniowo czynnych wzrost temperatury prowadzi do zmniejszenia wartości CMC i znacznego wzrostu objętości miceli, więc jasne jest, że odpowiedni wzrost temperatury pomoże niejonowym środkowi powierzchniowo czynnym wywierać działanie powierzchniowo aktywne. Jednak temperatura nie powinna przekraczać punktu chmur.
Krótko mówiąc, optymalna temperatura mycia zależy od sformułowania detergentu i mycia obiektu. Niektóre detergenty mają dobry efekt detergentu w temperaturze pokojowej, podczas gdy inne mają zupełnie inny detergencja między zimnym i gorącym myciem.
③ Piana
Zwyczajowe jest mycie siły pienionej z efektem mycia, wierząc, że detergenty o wysokiej mocy pienionej mają dobry efekt mycia. Badania wykazały, że nie ma bezpośredniego związku między efektem mycia a ilością pianki. Na przykład pranie z detergentami o niskiej pieniących się jest nie mniej skuteczne niż mycie detergentami o wysokim pieniącym poziomie.
Chociaż piana nie jest bezpośrednio związana z myciem, zdarza się, że pomaga usunąć brud, na przykład podczas mycia naczyń ręcznych. Podczas szorowania dywanów piana może również usunąć kurz i inne stałe cząsteczki brudu, dywan dywany odpowiada za dużą część pyłu, więc środki czyszczenia dywanów powinny mieć pewną zdolność pieniaka.
Moc pieniona jest również ważna dla szamponów, gdzie drobna piana wytwarzana przez płyn podczas szamponu lub kąpieli pozostawia włosy smarowane i wygodne.
④ Odmiany włókien i właściwości fizycznych tekstyliów
Oprócz struktury chemicznej włókien, która wpływa na przyczepność i usuwanie brudu, pojawienie się włókien oraz organizacji przędzy i tkaniny mają wpływ na łatwość usuwania brudu.
Skale włókien wełnianych i zakrzywione płaskie wstążki włókien bawełnianych częściej gromadzą brud niż włókna gładkie. Na przykład sadza zabarwiona filmami celulozowymi (filmy wiskozowe) jest łatwe do usunięcia, podczas gdy sadowa czarna zabarwiona tkaniną bawełnianą jest trudna do zmycia. Innym przykładem jest to, że tkaniny z krótkimi włókien wykonane z poliestrowego są bardziej podatne na gromadzenie plam oleju niż tkaniny o długim włóknie, a plamy olejowe na tkaninach krótkofalowych są również trudniejsze do usunięcia niż plamy oleju na tkaninach o długim błędy.
Ciasno skręcone przędzy i ciasne tkaniny, ze względu na niewielką szczelinę między włókienami, mogą oprzeć się inwazji brudu, ale to samo może zapobiec praniu cieczom wykluczenia wewnętrznego brudu, więc ciasne tkaniny zaczynają opierać się brudowi, ale kiedyś poplamione mycie jest również trudniejsze.
⑤ Twardość wody
Stężenie jonów Ca2+, Mg2+ i innych metali w wodzie ma duży wpływ na efekt mycia, szczególnie gdy anionowe środki powierzchniowo czynne napotykają jony Ca2+ i Mg2+ tworzące sole wapnia i magnezu, które są mniej rozpuszczalne i zmniejszą jego detergencję. W twardej wodzie, nawet jeśli stężenie środka powierzchniowo czynnego jest wysokie, detergencja jest nadal znacznie gorsza niż w destylacji. Aby surfaktant miał najlepszy efekt prania, stężenie jonów Ca2+ w wodzie należy zmniejszyć do 1 x 10-6 mol/l (CACO3 do 0,1 mg/l) lub mniej. Wymaga to dodania różnych zmiękczających do detergentu.
Czas po: 25-2022 lutego



