Spis treści tego artykułu:
1. Rozwój aminokwasów
2. Właściwości strukturalne
3. Skład chemiczny
4. Klasyfikacja
5. Synteza
6. Właściwości fizykochemiczne
7. Toksyczność
8. Działanie przeciwdrobnoustrojowe
9. Właściwości reologiczne
10. Zastosowania w przemyśle kosmetycznym
11. Zastosowania w kosmetyce codziennej
Aminokwasowe środki powierzchniowo czynne (AAS)to klasa środków powierzchniowo czynnych utworzonych przez połączenie grup hydrofobowych z jednym lub większą liczbą aminokwasów.W tym przypadku aminokwasy mogą być syntetyczne lub pochodzić z hydrolizatów białkowych lub podobnych źródeł odnawialnych.Ten artykuł zawiera szczegółowe informacje na temat większości dostępnych dróg syntezy AAS oraz wpływu różnych dróg na właściwości fizykochemiczne produktów końcowych, w tym rozpuszczalność, stabilność dyspersji, toksyczność i biodegradowalność.Jako klasa surfaktantów o rosnącym popycie, wszechstronność AAS ze względu na ich zmienną strukturę oferuje dużą liczbę możliwości komercyjnych.
Biorąc pod uwagę, że środki powierzchniowo czynne są szeroko stosowane w detergentach, emulgatorach, inhibitorach korozji, olejach trzeciorzędowych i farmaceutykach, naukowcy nigdy nie przestali zwracać uwagi na środki powierzchniowo czynne.
Surfaktanty to najbardziej reprezentatywne produkty chemiczne, które są codziennie spożywane w dużych ilościach na całym świecie i mają negatywny wpływ na środowisko wodne.Badania wykazały, że powszechne stosowanie tradycyjnych środków powierzchniowo czynnych może mieć negatywny wpływ na środowisko.
Obecnie nietoksyczność, biodegradowalność i biozgodność są dla konsumentów prawie tak samo ważne jak użyteczność i działanie środków powierzchniowo czynnych.
Biosurfaktanty to przyjazne dla środowiska, zrównoważone środki powierzchniowo czynne, które są naturalnie syntetyzowane przez mikroorganizmy, takie jak bakterie, grzyby i drożdże, lub wydzielane pozakomórkowo.W związku z tym biosurfaktanty można również wytwarzać za pomocą projektu molekularnego, aby naśladować naturalne struktury amfifilowe, takie jak fosfolipidy, alkiloglikozydy i acyloaminokwasy.
Surfaktanty aminokwasowe (AAS)należą do typowych środków powierzchniowo czynnych, zwykle wytwarzanych z surowców pochodzenia zwierzęcego lub rolnego.W ciągu ostatnich dwóch dekad AAS wzbudziły duże zainteresowanie naukowców jako nowe środki powierzchniowo czynne, nie tylko dlatego, że można je syntetyzować z zasobów odnawialnych, ale także dlatego, że AAS łatwo ulegają rozkładowi i mają nieszkodliwe produkty uboczne, dzięki czemu są bezpieczniejsze dla środowisko.
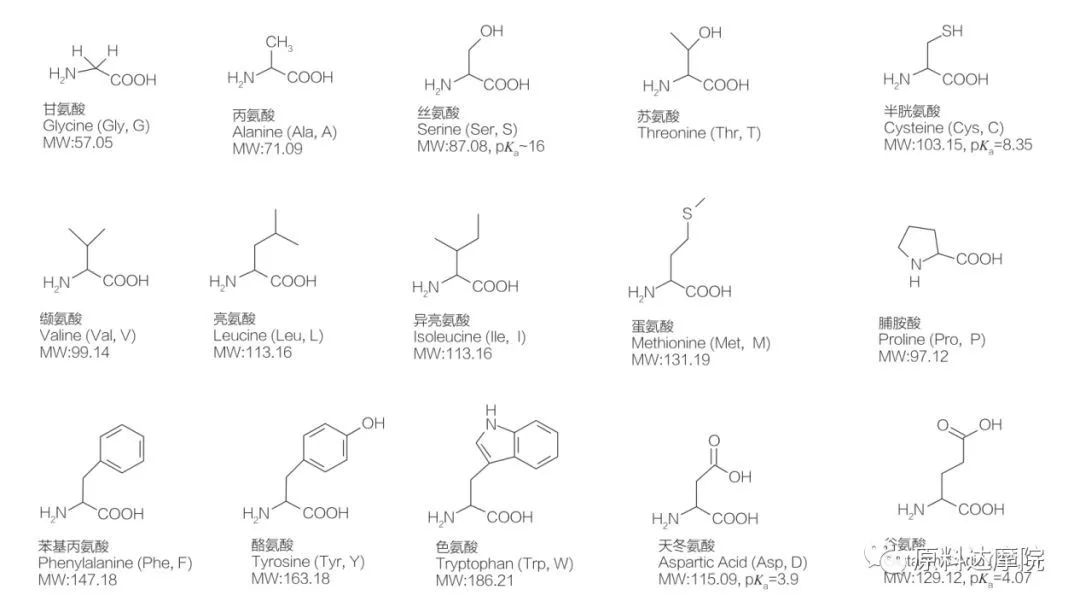
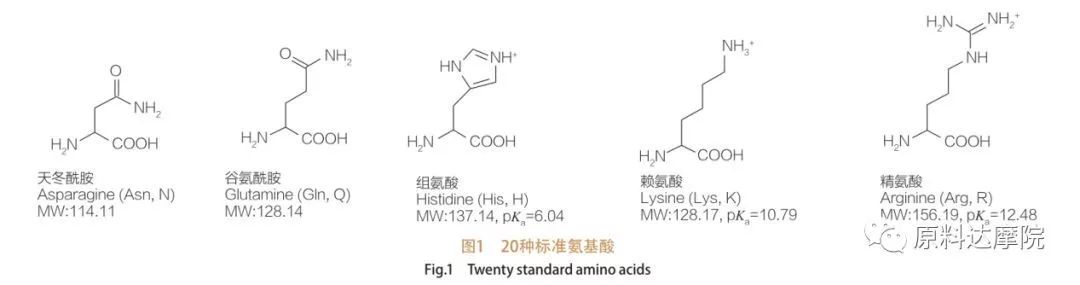
AAS można zdefiniować jako klasę środków powierzchniowo czynnych składającą się z aminokwasów zawierających grupy aminokwasowe (HO 2 C-CHR-NH 2) lub reszty aminokwasowe (HO 2 C-CHR-NH-).2 funkcjonalne regiony aminokwasów pozwalają na wyprowadzenie szerokiej gamy środków powierzchniowo czynnych.Wiadomo, że w naturze występuje łącznie 20 standardowych aminokwasów proteinogennych, które są odpowiedzialne za wszystkie reakcje fizjologiczne podczas wzrostu i aktywności życiowej.Różnią się one od siebie tylko resztą R (Rysunek 1, pk a jest ujemnym logarytmem stałej dysocjacji kwasu roztworu).Niektóre są niepolarne i hydrofobowe, inne polarne i hydrofilowe, niektóre zasadowe, a jeszcze inne kwaśne.
Ponieważ aminokwasy są związkami odnawialnymi, środki powierzchniowo czynne syntetyzowane z aminokwasów mają również duży potencjał, aby stać się zrównoważonymi i przyjaznymi dla środowiska.Prosta i naturalna struktura, niska toksyczność i szybka biodegradowalność często czynią je lepszymi od konwencjonalnych środków powierzchniowo czynnych.Wykorzystując surowce odnawialne (np. aminokwasy i oleje roślinne), AAS można wytwarzać różnymi drogami biotechnologicznymi i chemicznymi.
Na początku XX wieku po raz pierwszy odkryto, że aminokwasy są stosowane jako substraty do syntezy środków powierzchniowo czynnych.SAA stosowane były głównie jako konserwanty w preparatach farmaceutycznych i kosmetycznych.Ponadto stwierdzono, że SAA są biologicznie aktywne przeciwko różnym chorobotwórczym bakteriom, nowotworom i wirusom.W 1988 roku dostępność tanich AAS wywołała zainteresowanie badawcze aktywnością powierzchniową.Obecnie, wraz z rozwojem biotechnologii, niektóre Aminokwasy mogą być również komercyjnie syntetyzowane na dużą skalę przez drożdże, co pośrednio dowodzi, że produkcja AAS jest bardziej przyjazna dla środowiska.
01 Rozwój aminokwasów
Już na początku XIX wieku, kiedy po raz pierwszy odkryto naturalnie występujące aminokwasy, przewidywano, że ich struktury będą niezwykle cenne - użyteczne jako surowce do wytwarzania amfifilów.Pierwsze badania nad syntezą SAA zostały opisane przez Bondiego w 1909 roku.
W tym badaniu N-acyloglicyna i N-acyloalanina zostały wprowadzone jako grupy hydrofilowe dla środków powierzchniowo czynnych.Późniejsze prace obejmowały syntezę lipoaminokwasów (AAS) przy użyciu glicyny i alaniny, a Hentrich i in.opublikował serię ustaleń,w tym pierwsze zgłoszenie patentowe, dotyczące stosowania soli acylosarkozynianu i acylu asparaginianu jako środków powierzchniowo czynnych w domowych produktach czyszczących (np. szamponach, detergentach i pastach do zębów).Następnie wielu naukowców badało syntezę i właściwości fizykochemiczne aminokwasów acylowych.Do tej pory opublikowano obszerną literaturę na temat syntezy, właściwości, zastosowań przemysłowych i biodegradowalności AAS.
02 Właściwości konstrukcyjne
Niepolarne hydrofobowe łańcuchy kwasów tłuszczowych AAS mogą różnić się budową, długością i liczbą łańcuchów.Różnorodność strukturalna i wysoka aktywność powierzchniowa SAA wyjaśniają ich szeroką różnorodność składu oraz właściwości fizykochemiczne i biologiczne.Główne grupy AAS składają się z aminokwasów lub peptydów.Różnice w grupach głównych determinują adsorpcję, agregację i aktywność biologiczną tych surfaktantów.Grupy funkcyjne w grupie głównej określają następnie typ SAA, w tym kationowy, anionowy, niejonowy i amfoteryczny.Połączenie hydrofilowych aminokwasów i hydrofobowych części długołańcuchowych tworzy strukturę amfifilową, która sprawia, że cząsteczka jest wysoce aktywna powierzchniowo.Ponadto obecność asymetrycznych atomów węgla w cząsteczce pomaga w tworzeniu cząsteczek chiralnych.
03 Skład chemiczny
Wszystkie peptydy i polipeptydy są produktami polimeryzacji tych prawie 20 α-proteinogennych α-aminokwasów.Wszystkie 20 α-aminokwasów zawiera grupę funkcyjną kwasu karboksylowego (-COOH) i grupę funkcyjną aminową (-NH 2), obie przyłączone do tego samego tetraedrycznego atomu węgla α.Aminokwasy różnią się między sobą różnymi grupami R przyłączonymi do węgla α (z wyjątkiem licyny, gdzie grupą R jest wodór). Grupy R mogą różnić się budową, wielkością i ładunkiem (kwasowość, zasadowość).Różnice te determinują również rozpuszczalność Aminokwasów w wodzie.
Aminokwasy są chiralne (z wyjątkiem glicyny) i są z natury aktywne optycznie, ponieważ mają cztery różne podstawniki połączone z węglem alfa.Aminokwasy mają dwie możliwe konformacje;są to nienakładające się na siebie lustrzane odbicia, pomimo faktu, że liczba L-stereoizomerów jest znacznie wyższa.Grupa R obecna w niektórych aminokwasach (fenyloalanina, tyrozyna i tryptofan) to aryl, co prowadzi do maksymalnej absorpcji UV przy 280 nm.Kwaśny α-COOH i zasadowy α-NH 2 w aminokwasach są zdolne do jonizacji, a oba stereoizomery, czymkolwiek są, konstruują równowagę jonizacji pokazaną poniżej.
R-COOH ↔R-COO-+H+
R-NH3+↔R-NH2+H+
Jak pokazano w powyższej równowadze jonizacji, aminokwasy zawierają co najmniej dwie słabo kwasowe grupy;jednak grupa karboksylowa jest znacznie bardziej kwaśna w porównaniu z protonowaną grupą aminową.pH 7,4, grupa karboksylowa jest deprotonowana, a grupa aminowa jest protonowana.Aminokwasy z niejonizującymi grupami R są elektrycznie obojętne przy tym pH i tworzą jon obojnaczy.
04 Klasyfikacja
SAA można sklasyfikować według czterech kryteriów, które kolejno opisano poniżej.
4.1 Według pochodzenia
| W zależności od pochodzenia AAS można podzielić na 2 kategorie w następujący sposób. ① Kategoria naturalna Niektóre naturalnie występujące związki zawierające aminokwasy mają również zdolność zmniejszania napięcia powierzchniowego/międzyfazowego, a niektóre nawet przewyższają skuteczność glikolipidów.Te SAA są również znane jako lipopeptydy.Lipopeptydy to związki o niskiej masie cząsteczkowej, zwykle wytwarzane przez gatunki Bacillus.
Takie SAA są dalej podzielone na 3 podklasy:surfaktyna, ituryna i fengycyna.
|
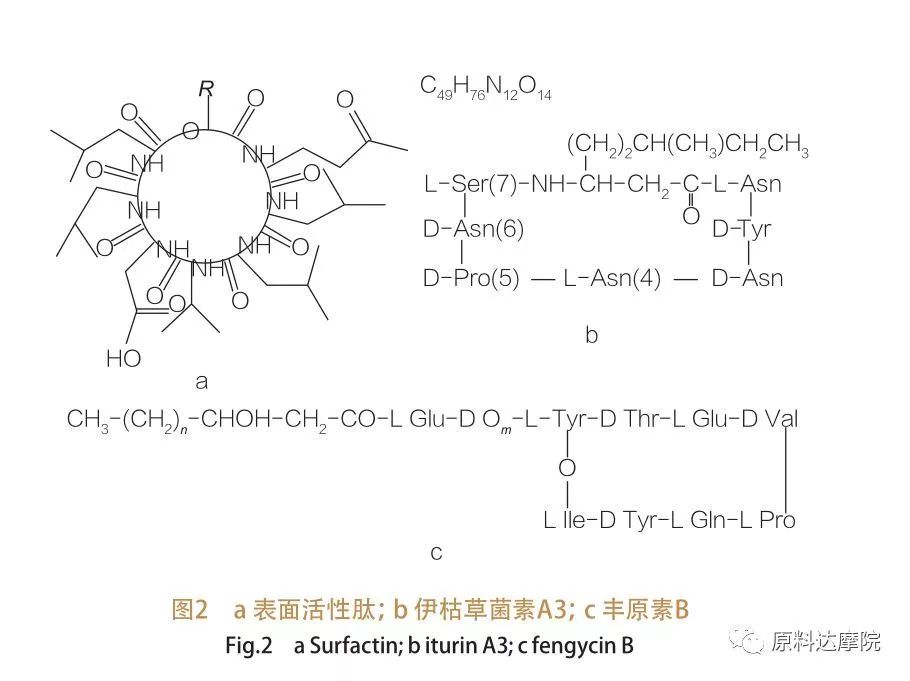
| Rodzina peptydów powierzchniowo czynnych obejmuje warianty heptapeptydowe różnych substancji,jak pokazano na Figurze 2a, na której łańcuch C12-C16 nienasyconego β-hydroksykwasu tłuszczowego jest połączony z peptydem.Peptyd powierzchniowo czynny jest makrocyklicznym laktonem, w którym pierścień jest zamknięty przez katalizę między C-końcem β-hydroksykwasu tłuszczowego i peptydem. W podklasie ituryny istnieje sześć głównych wariantów, a mianowicie ituryna A i C, mykosubtylina i bacillomycyna D, F i L.We wszystkich przypadkach heptapeptydy są połączone z łańcuchami C14-C17 β-aminokwasów tłuszczowych (łańcuchy mogą być różne).W przypadku ekurimycyn grupa aminowa w pozycji β może tworzyć wiązanie amidowe z C-końcem, tworząc makrocykliczną strukturę laktamową.
Podklasa fengycyny zawiera fengycynę A i B, które są również nazywane plipastatyną, gdy Tyr9 ma konfigurację D.Dekapeptyd jest połączony z nasyconym lub nienasyconym łańcuchem β-hydroksykwasu tłuszczowego C14-C18.Strukturalnie plipastatyna jest również makrocyklicznym laktonem, zawierającym boczny łańcuch Tyr w pozycji 3 sekwencji peptydowej i tworzącym wiązanie estrowe z resztą C-końcową, tworząc w ten sposób wewnętrzną strukturę pierścieniową (jak w przypadku wielu lipopeptydów Pseudomonas).
② Kategoria syntetyczna AAS można również syntetyzować przy użyciu dowolnego z kwaśnych, zasadowych i obojętnych aminokwasów.Typowymi aminokwasami używanymi do syntezy AAS są kwas glutaminowy, seryna, prolina, kwas asparaginowy, glicyna, arginina, alanina, leucyna i hydrolizaty białkowe.Tę podklasę środków powierzchniowo czynnych można wytworzyć metodami chemicznymi, enzymatycznymi i chemoenzymatycznymi;jednak w przypadku produkcji SAA synteza chemiczna jest bardziej ekonomicznie wykonalna.Typowe przykłady obejmują kwas N-lauroilo-L-glutaminowy i kwas N-palmitoilo-L-glutaminowy.
|
4.2 Na podstawie alifatycznych podstawników łańcuchowych
W oparciu o podstawniki łańcucha alifatycznego surfaktanty na bazie aminokwasów można podzielić na 2 rodzaje.
Zgodnie z pozycją podstawnika
| ①N-podstawiony AAS W związkach N-podstawionych grupa aminowa jest zastępowana przez grupę lipofilową lub grupę karboksylową, co powoduje utratę zasadowości.najprostszym przykładem N-podstawionych AAS są N-acyloaminokwasy, które są zasadniczo anionowymi środkami powierzchniowo czynnymi.n-podstawione AAS mają wiązanie amidowe przyłączone między częścią hydrofobową i hydrofilową.Wiązanie amidowe ma zdolność tworzenia wiązania wodorowego, co ułatwia degradację tego środka powierzchniowo czynnego w środowisku kwaśnym, czyniąc go biodegradowalnym.
② AAS podstawiony C W związkach C-podstawionych podstawienie zachodzi na grupie karboksylowej (poprzez wiązanie amidowe lub estrowe).Typowe związki C-podstawione (np. estry lub amidy) są zasadniczo kationowymi środkami powierzchniowo czynnymi.
③N- i C-podstawiony AAS W tego typu surfaktantach zarówno grupa aminowa, jak i karboksylowa są częścią hydrofilową.Ten typ jest zasadniczo amfoterycznym środkiem powierzchniowo czynnym. |
4.3 Według liczby hydrofobowych ogonów
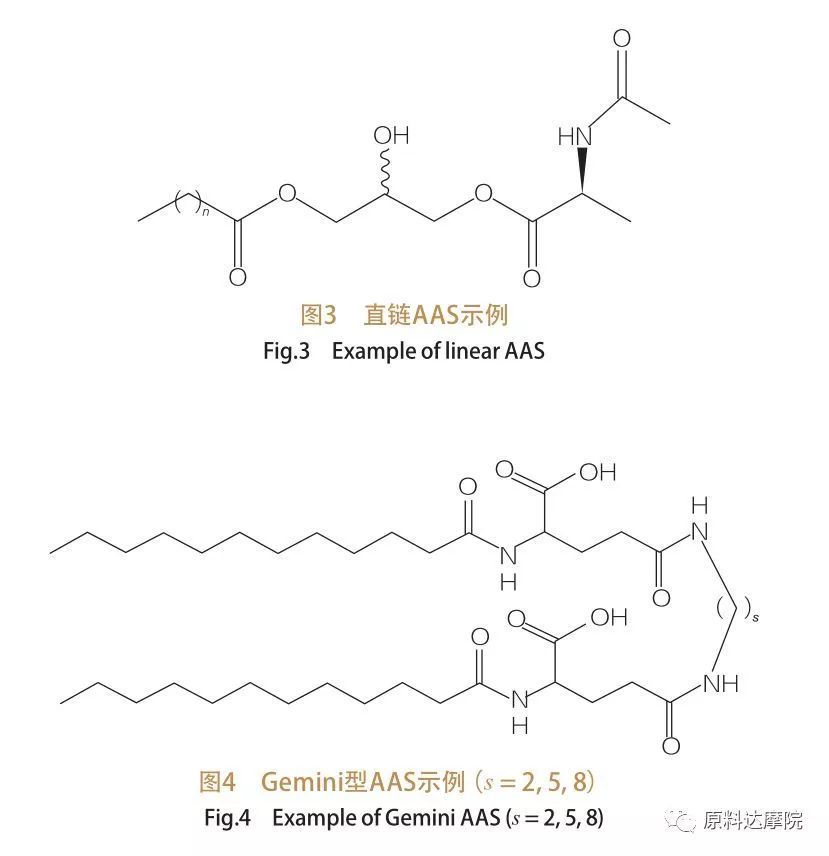
Na podstawie liczby grup głów i hydrofobowych ogonów SAA można podzielić na cztery grupy.Prostołańcuchowy AAS, Gemini (dimer) typu AAS, glicerolipidowy typ AAS i dwugłowy amfifilowy (Bola) typ AAS.prostołańcuchowe środki powierzchniowo czynne to środki powierzchniowo czynne składające się z aminokwasów z tylko jednym hydrofobowym ogonem (ryc. 3).AAS typu Gemini mają dwie polarne grupy aminokwasów i dwa hydrofobowe ogony na cząsteczkę (ryc. 4).W tego typu strukturze dwa proste łańcuchy AAS są połączone ze sobą przekładką i dlatego są również nazywane dimerami.Z drugiej strony, w AAS typu glicerolipidowego dwa hydrofobowe ogony są przyłączone do tej samej grupy aminokwasowej głowy.Te środki powierzchniowo czynne można uznać za analogi monoglicerydów, diglicerydów i fosfolipidów, podczas gdy w AAS typu Bola dwie główne grupy aminokwasów są połączone hydrofobowym ogonem.
4.4 W zależności od rodzaju grupy głównej
①Kationowe SAA
Głowna grupa tego typu środka powierzchniowo czynnego ma ładunek dodatni.Najwcześniejszym kationowym SAA jest arginian kokoilu etylu, który jest karboksylanem pirolidonu.Unikalne i różnorodne właściwości tego środka powierzchniowo czynnego sprawiają, że jest on przydatny w środkach dezynfekujących, przeciwdrobnoustrojowych, antystatycznych, odżywkach do włosów, a także jest łagodny dla oczu i skóry oraz łatwo ulega biodegradacji.Singare i Mhatre zsyntetyzowali kationowe SAA na bazie argininy i ocenili ich właściwości fizykochemiczne.W tym badaniu stwierdzili wysokie wydajności produktów otrzymanych w warunkach reakcji Schottena-Baumanna.Stwierdzono, że wraz ze wzrostem długości łańcucha alkilowego i hydrofobowości aktywność powierzchniowa środka powierzchniowo czynnego wzrasta, a krytyczne stężenie miceli (cmc) maleje.Kolejnym jest czwartorzędowe białko acylowe, które jest powszechnie stosowane jako odżywka w produktach do pielęgnacji włosów.
② Anionowy AAS
W anionowych środkach powierzchniowo czynnych polarna grupa głowy środka powierzchniowo czynnego ma ładunek ujemny.Sarkozyna (CH 3-NH-CH 2-COOH, N-metyloglicyna), aminokwas powszechnie występujący w jeżowcach i rozgwiazdach, jest chemicznie spokrewniona z glicyną (NH 2-CH 2-COOH), aminokwasem zasadowym występującym w komórkach ssaków.-COOH,) jest chemicznie spokrewniony z glicyną, która jest podstawowym aminokwasem występującym w komórkach ssaków.Kwas laurynowy, kwas tetradekanowy, kwas oleinowy oraz ich halogenki i estry są powszechnie stosowane do syntezy sarkozynianowych środków powierzchniowo czynnych.Sarkozyniany są z natury łagodne i dlatego są powszechnie stosowane w płynach do płukania ust, szamponach, piankach do golenia w sprayu, filtrach przeciwsłonecznych, środkach do czyszczenia skóry i innych produktach kosmetycznych.
Inne dostępne w handlu anionowe SAA obejmują Amisoft CS-22 i AmiliteGCK-12, które są nazwami handlowymi odpowiednio N-kokoilo-L-glutaminianu sodu i N-kokoiloglicynianu potasu.Amilit jest powszechnie stosowany jako środek pieniący, detergent, solubilizator, emulgator i środek dyspergujący i ma wiele zastosowań w kosmetykach, takich jak szampony, mydła do kąpieli, płyny do mycia ciała, pasty do zębów, środki do mycia twarzy, mydła oczyszczające, środki do czyszczenia soczewek kontaktowych i domowe środki powierzchniowo czynne.Amisoft jest stosowany jako łagodny środek do mycia skóry i włosów, głównie w środkach do mycia twarzy i ciała, syntetycznych detergentach blokowych, produktach do pielęgnacji ciała, szamponach i innych produktach do pielęgnacji skóry.
③AAS obojniaczojonowy lub amfoteryczny
Amfoteryczne środki powierzchniowo czynne zawierają zarówno miejsca kwasowe, jak i zasadowe, dlatego mogą zmieniać swój ładunek, zmieniając wartość pH.W środowisku alkalicznym zachowują się jak surfaktanty anionowe, w środowisku kwaśnym jak surfaktanty kationowe, aw środowisku obojętnym jak surfaktanty amfoteryczne.Laurylolizyna (LL) i alkoksy(2-hydroksypropylo)arginina to jedyne znane amfoteryczne środki powierzchniowo czynne na bazie aminokwasów.LL jest produktem kondensacji lizyny i kwasu laurynowego.Ze względu na swoją amfoteryczną strukturę LL jest nierozpuszczalny w prawie wszystkich typach rozpuszczalników, z wyjątkiem bardzo zasadowych lub kwaśnych rozpuszczalników.Jako proszek organiczny LL ma doskonałą przyczepność do powierzchni hydrofilowych i niski współczynnik tarcia, co nadaje temu surfaktantowi doskonałe właściwości smarne.LL jest szeroko stosowany w kremach do skóry i odżywkach do włosów, a także jako lubrykant.
④Niejonowe AAS
Niejonowe środki powierzchniowo czynne charakteryzują się polarnymi grupami głównymi bez ładunków formalnych.osiem nowych etoksylowanych niejonowych środków powierzchniowo czynnych zostało przygotowanych przez Al-Sabagh i in.z rozpuszczalnych w tłuszczach α-aminokwasów.W tym procesie L-fenyloalanina (LEP) i L-leucyna zostały najpierw zestryfikowane heksadekanolem, a następnie amidowane kwasem palmitynowym, w wyniku czego otrzymano dwa amidy i dwa estry α-aminokwasów.Amidy i estry poddano następnie reakcjom kondensacji z tlenkiem etylenu, w wyniku czego otrzymano trzy pochodne fenyloalaniny o różnej liczbie jednostek polioksyetylenowych (40, 60 i 100).Stwierdzono, że te niejonowe AAS mają dobre właściwości piorące i pieniące.
05 Synteza
5.1 Podstawowa droga syntezy
W AAS grupy hydrofobowe mogą być przyłączone do miejsc aminowych lub karboksylowych lub poprzez łańcuchy boczne aminokwasów.Na tej podstawie dostępne są cztery podstawowe drogi syntezy, jak pokazano na rysunku 5.
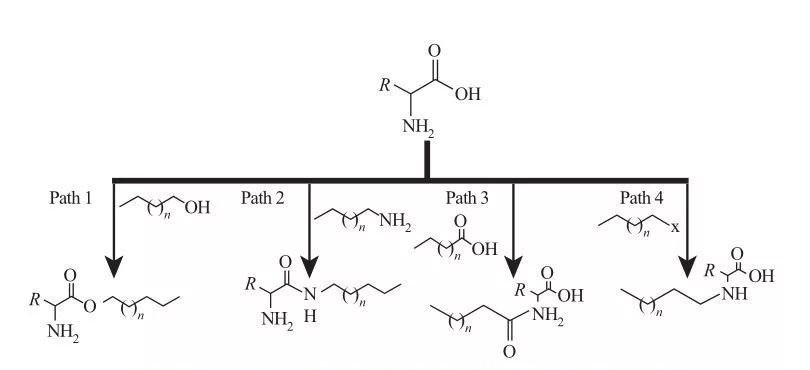
Ryc.5 Podstawowe ścieżki syntezy surfaktantów na bazie aminokwasów
| Ścieżka 1. Amfifilowe estry aminy są wytwarzane w reakcjach estryfikacji, w którym to przypadku syntezę środka powierzchniowo czynnego uzyskuje się zwykle przez ogrzewanie pod chłodnicą zwrotną alkoholi tłuszczowych i aminokwasów w obecności środka odwadniającego i kwaśnego katalizatora.W niektórych reakcjach kwas siarkowy działa zarówno jako katalizator, jak i środek odwadniający.
Ścieżka 2. Aktywowane aminokwasy reagują z alkiloaminami, tworząc wiązania amidowe, w wyniku czego dochodzi do syntezy amfifilowych amidoamin.
Ścieżka 3. Amidokwasy są syntetyzowane w reakcji grup aminowych aminokwasów z aminokwasami.
Ścieżka 4. Długołańcuchowe aminokwasy alkilowe zsyntetyzowano w reakcji grup aminowych z haloalkanami. |
5.2 Postępy w syntezie i produkcji
5.2.1 Synteza surfaktantów jednołańcuchowych aminokwasów/peptydów
N-acylo lub O-acyloaminokwasy lub peptydy można syntetyzować przez katalizowane enzymatycznie acylowanie grup aminowych lub hydroksylowych kwasami tłuszczowymi.Najwcześniejsze doniesienia o bezrozpuszczalnikowej katalizowanej lipazą syntezie amidów aminokwasów lub pochodnych estrów metylowych wykorzystywały Candida antarctica z wydajnością w zakresie od 25% do 90% w zależności od docelowego aminokwasu.Keton metylowo-etylowy był również stosowany jako rozpuszczalnik w niektórych reakcjach.Vonderhagena i in.opisali także katalizowane lipazą i proteazą reakcje N-acylowania aminokwasów, hydrolizatów białkowych i/lub ich pochodnych z użyciem mieszaniny wody i rozpuszczalników organicznych (np. dimetyloformamid/woda) i ketonu metylowo-butylowego.
Na początku głównym problemem związanym z katalizowaną enzymatycznie syntezą AAS była niska wydajność.Według Valivety'ego i in.wydajność pochodnych aminokwasów N-tetradekanoilu wynosiła tylko 2%-10%, nawet po zastosowaniu różnych lipaz i inkubacji w temperaturze 70°C przez wiele dni.Monteta i in.napotkali również problemy związane z niską wydajnością aminokwasów w syntezie N-acylolizyny z wykorzystaniem kwasów tłuszczowych i olejów roślinnych.Według nich maksymalna wydajność produktu wyniosła 19% w warunkach bezrozpuszczalnikowych i przy użyciu rozpuszczalników organicznych.ten sam problem napotkali Valivety i in.w syntezie pochodnych estru metylowego N-Cbz-L-lizyny lub N-Cbz-lizyny.
W tym badaniu stwierdzili, że wydajność 3-O-tetradekanoilo-L-seryny wynosiła 80% przy użyciu N-zabezpieczonej seryny jako substratu i Novozyme 435 jako katalizatora w stopionym środowisku wolnym od rozpuszczalników.Nagao i Kito badali O-acylację L-seryny, L-homoseryny, L-treoniny i L-tyrozyny (LET) przy użyciu lipazy Wyniki reakcji (lipazę otrzymano z Candida cylindracea i Rhizopus delemar w wodnym środowisku buforowym) i poinformowali, że wydajności acylowania L-homoseryny i L-seryny były nieco niskie, podczas gdy nie wystąpiło acylowanie L-treoniny i LET.
Wielu badaczy poparło wykorzystanie niedrogich i łatwo dostępnych substratów do syntezy opłacalnych AAS.Soo i in.stwierdzili, że preparat surfaktantów na bazie oleju palmowego najlepiej działa z unieruchomionym lipoenzymem.Zauważyli, że wydajność produktów byłaby lepsza pomimo czasochłonnej reakcji (6 dni).Gerowa i in.badali syntezę i aktywność powierzchniową chiralnego N-palmitoilo AAS na bazie metioniny, proliny, leucyny, treoniny, fenyloalaniny i fenyloglicyny w mieszaninie cyklicznej/racemicznej.Pang i Chu opisali syntezę monomerów na bazie aminokwasów i monomerów na bazie kwasu dikarboksylowego w roztworze Szereg funkcjonalnych i biodegradowalnych estrów poliamidowych na bazie aminokwasów zsyntetyzowano w reakcjach współkondensacji w roztworze.
Cantaeuzene i Guerreiro opisali estryfikację grup kwasów karboksylowych Boc-Ala-OH i Boc-Asp-OH długołańcuchowymi alkoholami alifatycznymi i diolami, z dichlorometanem jako rozpuszczalnikiem i agarozą 4B (Sepharose 4B) jako katalizatorem.W tym badaniu reakcja Boc-Ala-OH z alkoholami tłuszczowymi do 16 atomów węgla dała dobrą wydajność (51%), podczas gdy dla Boc-Asp-OH 6 i 12 atomów węgla była lepsza, z odpowiednią wydajnością 63% [64 ].99,9%) z wydajnością w zakresie od 58% do 76%, które zostały zsyntetyzowane przez utworzenie wiązań amidowych z różnymi długołańcuchowymi alkiloaminami lub wiązań estrowych z alkoholami tłuszczowymi przez Cbz-Arg-OMe, gdzie papaina działała jako katalizator.
5.2.2 Synteza surfaktantów aminokwasowych/peptydowych na bazie gemini
Surfaktanty gemini na bazie aminokwasów składają się z dwóch cząsteczek AAS o prostym łańcuchu połączonych ze sobą łeb w łeb za pomocą grupy rozdzielającej.Istnieją 2 możliwe schematy chemoenzymatycznej syntezy środków powierzchniowo czynnych na bazie aminokwasów typu gemini (ryc. 6 i 7).Na fig. 6, 2 pochodne aminokwasów poddaje się reakcji ze związkiem jako grupą oddzielającą, a następnie wprowadza się 2 grupy hydrofobowe.Na rycinie 7 2 prostołańcuchowe struktury są bezpośrednio połączone ze sobą za pomocą dwufunkcyjnej grupy rozdzielającej.
Najwcześniejszy rozwój katalizowanej enzymami syntezy gemini lipoaminokwasów został zapoczątkowany przez Valivety i in.Yoshimura i in.badali syntezę, adsorpcję i agregację gemini surfaktantu na bazie aminokwasów na bazie cystyny i bromku n-alkilu.Zsyntetyzowane środki powierzchniowo czynne porównano z odpowiednimi monomerycznymi środkami powierzchniowo czynnymi.Faustino i in.opisali syntezę anionowego monomerycznego AAS na bazie mocznika na bazie L-cystyny, D-cystyny, DL-cystyny, L-cysteiny, L-metioniny i L-sulfoalaniny oraz ich par gemini za pomocą przewodnictwa, równowagi napięcia powierzchniowego i stałego -stanowa ich charakterystyka fluorescencyjna.Wykazano, że wartość cmc gemini była niższa przez porównanie monomeru i gemini.
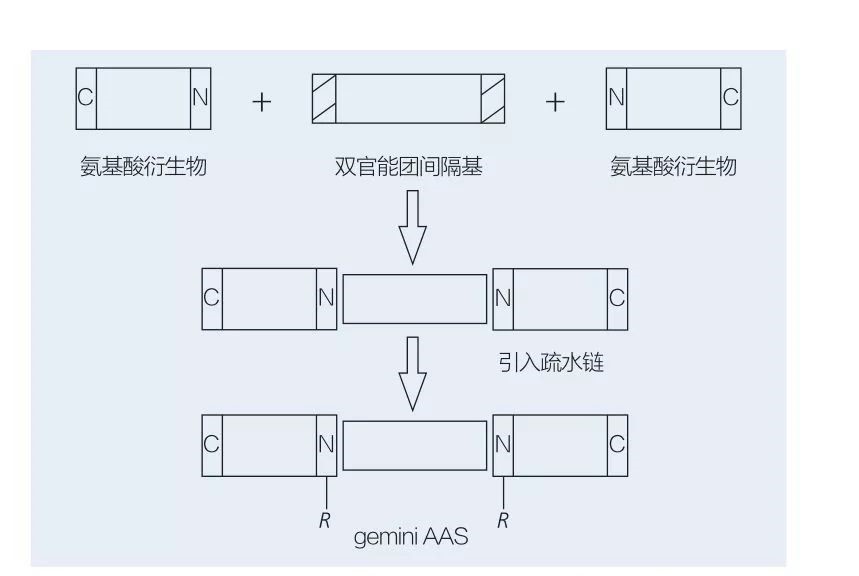
Ryc. 6 Synteza gemini AAS przy użyciu pochodnych AA i odstępnika, a następnie wstawienie grupy hydrofobowej
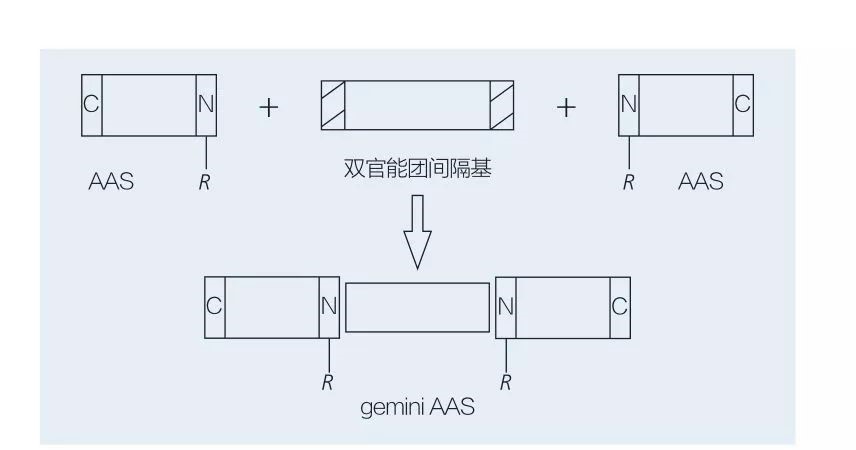
Ryc. 7 Synteza gemini AAS przy użyciu dwufunkcyjnego odstępnika i AAS
5.2.3 Synteza glicerolipidowych aminokwasów/peptydów powierzchniowo czynnych
Glicerolipidowe aminokwasy/peptydowe środki powierzchniowo czynne to nowa klasa aminokwasów lipidowych, które są strukturalnymi analogami mono- (lub die) estrów i fosfolipidów glicerolu, ze względu na ich strukturę jednego lub dwóch łańcuchów tłuszczowych z jednym aminokwasem połączonym ze szkieletem glicerolu przez wiązanie estrowe.Syntezę tych surfaktantów rozpoczyna się od przygotowania estrów glicerolowych aminokwasów w podwyższonej temperaturze iw obecności kwaśnego katalizatora (np. BF 3).Dobrym rozwiązaniem jest również synteza katalizowana enzymatycznie (z wykorzystaniem hydrolaz, proteaz i lipaz jako katalizatorów) (Rysunek 8).
Opisano katalizowaną enzymem syntezę koniugatów dilaurylowanych glicerydów argininy z użyciem papainy.Opisano również syntezę koniugatów estrów diacyloglicerolu z acetyloargininy oraz ocenę ich właściwości fizykochemicznych.
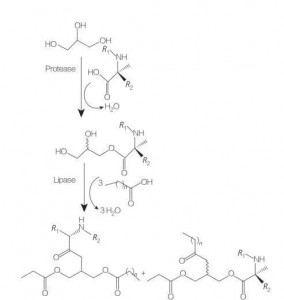
Ryc. 8 Synteza koniugatów aminokwasowych mono i diacyloglicerolu
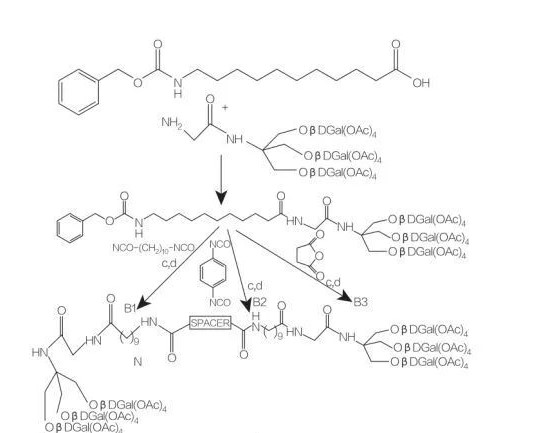
odstępnik: NH-(CH2)10-NH: związek B1
przekładka: NH-C6H4-NH: związek B2
przekładka: CH2-CH2: związek B3
Ryc.9 Synteza symetrycznych związków amfifilowych pochodzących z tris(hydroksymetylo)aminometanu
5.2.4 Synteza środków powierzchniowo czynnych na bazie aminokwasów/peptydów
Amfifile typu bola na bazie aminokwasów zawierają 2 aminokwasy, które są połączone z tym samym łańcuchem hydrofobowym.Franceschi i in.opisali syntezę amfifilów typu bola z 2 aminokwasami (D- lub L-alaniną lub L-histydyną) i 1 łańcuchem alkilowym o różnej długości i zbadali ich aktywność powierzchniową.Omawiają syntezę i agregację nowych amfifilów typu bola z frakcją aminokwasową (przy użyciu rzadkiego β-aminokwasu lub alkoholu) i grupą rozdzielającą C12-C20.Niezwykłymi stosowanymi β-aminokwasami mogą być aminokwas cukrowy, aminokwas pochodzący z azydotyminy (AZT), aminokwas norbornenowy i aminoalkohol pochodzący z AZT (ryc. 9).synteza symetrycznych związków amfifilowych typu bola pochodzących z tris(hydroksymetylo)aminometanu (Tris) (ryc. 9).
06 Właściwości fizykochemiczne
Powszechnie wiadomo, że środki powierzchniowo czynne na bazie aminokwasów (AAS) są różnorodne i wszechstronne w naturze i mają dobre zastosowanie w wielu zastosowaniach, takich jak dobra rozpuszczalność, dobre właściwości emulgujące, wysoka wydajność, wysoka aktywność powierzchniowa i dobra odporność na twardą wodę (jon wapnia tolerancja).
Na podstawie właściwości powierzchniowo czynnych aminokwasów (np. napięcie powierzchniowe, cmc, zachowanie fazowe i temperatura Kraffta), po szeroko zakrojonych badaniach wyciągnięto następujące wnioski - aktywność powierzchniowa SAA jest lepsza niż jego konwencjonalnego odpowiednika środka powierzchniowo czynnego.
6.1 Krytyczne stężenie miceli (cmc)
Krytyczne stężenie miceli jest jednym z ważnych parametrów surfaktantów i reguluje wiele właściwości powierzchniowo czynnych, takich jak solubilizacja, liza komórek i ich interakcja z biofilmami itp. Ogólnie rzecz biorąc, zwiększenie długości łańcucha ogona węglowodorowego (zwiększenie hydrofobowości) prowadzi do zmniejszenia w wartości cmc roztworu środka powierzchniowo czynnego, zwiększając w ten sposób jego aktywność powierzchniową.Surfaktanty oparte na aminokwasach mają zwykle niższe wartości cmc w porównaniu do konwencjonalnych surfaktantów.
Poprzez różne kombinacje grup głównych i hydrofobowych ogonów (amid mono-kationowy, amid bi-kationowy, ester na bazie amidu bi-kationowego), Infante i in.zsyntetyzowali trzy AAS na bazie argininy i zbadali ich cmc i γcmc (napięcie powierzchniowe w cmc), wykazując, że wartości cmc i γcmc zmniejszały się wraz ze wzrostem hydrofobowej długości ogona.W innym badaniu Singare i Mhatre stwierdzili, że cmc surfaktantów N-α-acylargininowych zmniejszało się wraz ze wzrostem liczby hydrofobowych atomów węgla w ogonie (Tabela 1).
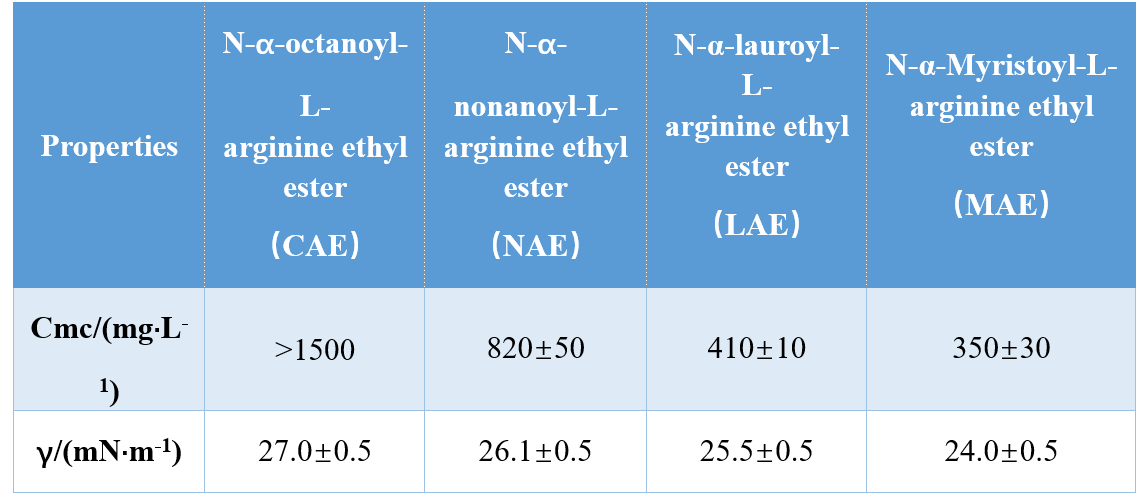
Yoshimura i in.zbadali cmc bliźniaczych środków powierzchniowo czynnych na bazie aminokwasów cysteiny i wykazali, że cmc zmniejszyło się, gdy długość łańcucha węglowego w łańcuchu hydrofobowym wzrosła z 10 do 12. Dalsze zwiększenie długości łańcucha węglowego do 14 spowodowało wzrost cmc, co potwierdziło, że długołańcuchowe gemini surfaktanty mają mniejszą tendencję do agregacji.
Faustino i in.opisali powstawanie mieszanych miceli w wodnych roztworach anionowych geminich surfaktantów na bazie cystyny.Surfaktanty gemini porównano również z odpowiednimi konwencjonalnymi surfaktantami monomerycznymi (C8 Cys).Wartości cmc mieszanin lipidów i surfaktantów były niższe niż czystych surfaktantów.surfaktanty gemini i 1,2-diheptanoilo-sn-glicerylo-3-fosfocholina, rozpuszczalny w wodzie, tworzący micele fosfolipid, miały cmc na poziomie milimolowym.
Shrestha i Aramaki badali powstawanie lepkosprężystych miceli przypominających robaki w wodnych roztworach mieszanych anionowo-niejonowych środków powierzchniowo czynnych na bazie aminokwasów przy braku domieszek soli.W tym badaniu stwierdzono, że glutaminian N-dodecylu ma wyższą temperaturę Kraffta;jednak po zneutralizowaniu zasadowym aminokwasem L-lizyną generował micele, a roztwór zaczął zachowywać się jak płyn newtonowski w temperaturze 25 ° C.
6.2 Dobra rozpuszczalność w wodzie
Dobra rozpuszczalność AAS w wodzie wynika z obecności dodatkowych wiązań CO-NH.To sprawia, że AAS są bardziej biodegradowalne i przyjazne dla środowiska niż odpowiadające im konwencjonalne środki powierzchniowo czynne.Rozpuszczalność w wodzie kwasu N-acylo-L-glutaminowego jest jeszcze lepsza ze względu na jego 2 grupy karboksylowe.Rozpuszczalność Cn(CA) 2 w wodzie jest również dobra, ponieważ w 1 cząsteczce znajdują się 2 jonowe grupy argininowe, co skutkuje skuteczniejszą adsorpcją i dyfuzją na styku komórek, a nawet skutecznym hamowaniem rozwoju bakterii przy niższych stężeniach.
6.3 Temperatura Kraffta i punkt Kraffta
Temperaturę Kraffta można rozumieć jako specyficzną rozpuszczalność środków powierzchniowo czynnych, których rozpuszczalność gwałtownie wzrasta powyżej określonej temperatury.Jonowe środki powierzchniowo czynne mają tendencję do tworzenia stałych hydratów, które mogą wytrącać się z wody.W określonej temperaturze (tzw. temperaturze Kraffta) zwykle obserwuje się gwałtowny i nieciągły wzrost rozpuszczalności surfaktantów.Punkt Kraffta jonowego środka powierzchniowo czynnego to jego temperatura Kraffta w cmc.
Ta charakterystyka rozpuszczalności jest zwykle obserwowana w przypadku jonowych środków powierzchniowo czynnych i można ją wyjaśnić w następujący sposób: rozpuszczalność monomeru wolnego od środka powierzchniowo czynnego jest ograniczona poniżej temperatury Kraffta aż do osiągnięcia punktu Kraffta, w którym jego rozpuszczalność stopniowo wzrasta z powodu tworzenia się miceli.Aby zapewnić pełną rozpuszczalność, konieczne jest przygotowanie preparatów surfaktantów w temperaturach powyżej punktu Kraffta.
Temperatura Kraffta AAS została zbadana i porównana z temperaturą konwencjonalnych syntetycznych środków powierzchniowo czynnych. Shrestha i Aramaki zbadali temperaturę Kraffta AAS na bazie argininy i stwierdzili, że krytyczne stężenie miceli wykazywało zachowanie agregacyjne w postaci pre-miceli powyżej 2-5 ×10-6 mol-L-1, a następnie tworzenie normalnych miceli (Ohta i wsp. zsyntetyzowali sześć różnych typów N-heksadekanoilowych AAS i omówili związek między ich temperaturą Kraffta a resztami aminokwasowymi.
W doświadczeniach stwierdzono, że temperatura Kraffta N-heksadekanoilu AAS wzrastała wraz ze zmniejszaniem się wielkości reszt aminokwasowych (wyjątkiem jest fenyloalanina), natomiast ciepło rozpuszczalności (pochłanianie ciepła) rosło wraz ze zmniejszaniem się wielkości reszt aminokwasowych (z z wyjątkiem glicyny i fenyloalaniny).Stwierdzono, że zarówno w układach alaninowych, jak i fenyloalaniny oddziaływanie DL jest silniejsze niż oddziaływanie LL w postaci stałej soli N-heksadekanoilo-AAS.
Brito i in.określili temperaturę Kraffta trzech serii nowych środków powierzchniowo czynnych na bazie aminokwasów za pomocą różnicowej mikrokalorymetrii skaningowej i stwierdzili, że zmiana jonu trifluorooctanowego na jon jodkowy spowodowała znaczny wzrost temperatury Kraffta (około 6 ° C), z 47 ° C do 53 ° C C.Obecność wiązań podwójnych cis i nienasycenie występujące w długołańcuchowych pochodnych Ser doprowadziła do znacznego obniżenia temperatury Kraffta.Doniesiono, że glutaminian n-dodecylu ma wyższą temperaturę Kraffta.Jednak neutralizacja zasadowym aminokwasem L-lizyną spowodowała utworzenie miceli w roztworze, które zachowywały się jak płyny newtonowskie w temperaturze 25°C.
6.4 Napięcie powierzchniowe
Napięcie powierzchniowe surfaktantów jest związane z długością łańcucha części hydrofobowej.Zhang i in.oznaczyli napięcie powierzchniowe kokoiloglicynianu sodu metodą płytkową Wilhelmy'ego (25±0,2)°C i wyznaczyli wartość napięcia powierzchniowego w cmc jako 33 mN-m -1 , cmc jako 0,21 mmol-L -1 .Yoshimura i in.wyznaczyli napięcie powierzchniowe środków powierzchniowo czynnych opartych na aminokwasach typu 2C n Cys opartych na 2C n Cys.Stwierdzono, że napięcie powierzchniowe w cmc zmniejszało się wraz ze wzrostem długości łańcucha (do n = 8), podczas gdy trend był odwrotny dla surfaktantów o n = 12 lub dłuższych długościach łańcucha.
Zbadano również wpływ CaC1 2 na napięcie powierzchniowe środków powierzchniowo czynnych na bazie aminokwasów dikarboksylowych.W badaniach tych CaCl 2 dodawano do wodnych roztworów trzech surfaktantów typu dikarboksylowanych aminokwasów (C12 MalNa 2, C12 AspNa 2 i C12 GluNa 2).Porównano wartości plateau po cmc i stwierdzono, że napięcie powierzchniowe zmniejsza się przy bardzo niskich stężeniach CaCl2.Wynika to z wpływu jonów wapnia na rozmieszczenie środka powierzchniowo czynnego na granicy faz gaz-woda.z drugiej strony, napięcia powierzchniowe soli N-dodecyloaminomalonianu i N-dodecylasparaginianu były również prawie stałe aż do stężenia 10 mmol-L-1 CaCl2.Powyżej 10 mmol-L-1 napięcie powierzchniowe gwałtownie wzrasta z powodu wytrącania się soli wapniowej środka powierzchniowo czynnego.W przypadku soli disodowej glutaminianu N-dodecylu umiarkowany dodatek CaC1 2 spowodował znaczny spadek napięcia powierzchniowego, natomiast dalszy wzrost stężenia CaC1 2 nie powodował już istotnych zmian.
Aby określić kinetykę adsorpcji AAS typu gemini na granicy faz gaz-woda, wyznaczono dynamiczne napięcie powierzchniowe metodą maksymalnego ciśnienia pęcherzyków.Wyniki pokazały, że przez najdłuższy czas testu dynamiczne napięcie powierzchniowe 2C 12 Cys nie uległo zmianie.Spadek dynamicznego napięcia powierzchniowego zależy tylko od stężenia, długości ogonów hydrofobowych i liczby ogonów hydrofobowych.Rosnące stężenie surfaktantu, zmniejszanie długości i liczby łańcuchów powodowało szybszy rozpad.Stwierdzono, że wyniki otrzymane dla wyższych stężeń Cn Cys (n = 8 do 12) są bardzo zbliżone do γ cmc zmierzonego metodą Wilhelmy'ego.
W innym badaniu dynamiczne napięcia powierzchniowe dilaurylosyny sodowej (SDLC) i didekaminocystyny sodowej oznaczano metodą płytkową Wilhelmy'ego, a ponadto równowagowe napięcia powierzchniowe ich roztworów wodnych oznaczano metodą objętości kropli.Reakcję wiązań dwusiarczkowych badano również innymi metodami.Dodatek merkaptoetanolu do 0,1 mmol-L-1SDLC doprowadził do gwałtownego wzrostu napięcia powierzchniowego z 34 mN-m-1 do 53 mN-m-1.Ponieważ NaClO może utleniać wiązania dwusiarczkowe SDLC do grup kwasu sulfonowego, po dodaniu NaClO (5 mmol-L-1) do roztworu SDLC o stężeniu 0,1 mmol-1-1 nie zaobserwowano żadnych agregatów.Wyniki transmisyjnej mikroskopii elektronowej i dynamicznego rozpraszania światła wykazały, że w roztworze nie powstały agregaty.Stwierdzono, że napięcie powierzchniowe SDLC wzrastało z 34 mN-m-1 do 60 mN-m-1 w ciągu 20 min.
6.5 Binarne oddziaływania powierzchniowe
W naukach przyrodniczych wiele grup badało właściwości wibracyjne mieszanin kationowych AAS (środków powierzchniowo czynnych na bazie diacyloglicerolu i argininy) i fosfolipidów na granicy faz gaz-woda, ostatecznie dochodząc do wniosku, że ta nieidealna właściwość powoduje występowanie oddziaływań elektrostatycznych.
6.6 Właściwości agregacji
Dynamiczne rozpraszanie światła jest powszechnie stosowane do określania właściwości agregacyjnych monomerów na bazie aminokwasów i surfaktantów gemini w stężeniach powyżej cmc, uzyskując pozorną średnicę hydrodynamiczną DH (= 2R H ).Agregaty utworzone przez Cn Cys i 2Cn Cys są stosunkowo duże i mają szeroki rozkład w skali w porównaniu z innymi środkami powierzchniowo czynnymi.Wszystkie środki powierzchniowo czynne z wyjątkiem 2C12 Cys zazwyczaj tworzą agregaty o wielkości około 10 nm.rozmiary miceli gemini środków powierzchniowo czynnych są znacznie większe niż ich monomerycznych odpowiedników.Wzrost długości łańcucha węglowodorowego prowadzi również do wzrostu wielkości miceli.ohta i in.opisali właściwości agregacyjne trzech różnych stereoizomerów N-dodecylo-fenylo-alanylo-fenylo-alaniny tetrametyloamoniowej w roztworze wodnym i wykazali, że diastereoizomery mają takie samo krytyczne stężenie agregacyjne w roztworze wodnym.Iwahashi i in.badano metodą dichroizmu kołowego, NMR i osmometrii ciśnieniowej pary Tworzenie chiralnych agregatów kwasu N-dodekanoilo-L-glutaminowego, N-dodekanoilo-L-waliny i ich estrów metylowych w różnych rozpuszczalnikach (takich jak tetrahydrofuran, acetonitryl, 1,4 -dioksan i 1,2-dichloroetan) o właściwościach rotacyjnych badano metodą dichroizmu kołowego, NMR i osmometrii prężnej pary.
6.7 Adsorpcja międzyfazowa
Jednym z kierunków badań jest również adsorpcja międzyfazowa surfaktantów na bazie aminokwasów i porównanie jej z jej konwencjonalnym odpowiednikiem.Na przykład zbadano właściwości adsorpcji międzyfazowej estrów dodecylowych aminokwasów aromatycznych otrzymanych z LET i LEP.Wyniki pokazały, że LET i LEP wykazywały mniejsze powierzchnie międzyfazowe odpowiednio na granicy faz gaz-ciecz i na granicy faz woda/heksan.
Bordes i in.zbadali zachowanie roztworu i adsorpcję na granicy faz gaz-woda trzech dikarboksylowanych aminokwasów surfaktantów, soli disodowych glutaminianu dodecylu, asparaginianu dodecylu i aminomalonianu (z odpowiednio 3, 2 i 1 atomem węgla między dwiema grupami karboksylowymi).Zgodnie z tym raportem cmc dikarboksylowanych środków powierzchniowo czynnych było 4-5 razy wyższe niż monokarboksylowanej soli dodecyloglicyny.Przypisuje się to tworzeniu wiązań wodorowych między dikarboksylowanymi środkami powierzchniowo czynnymi a sąsiednimi cząsteczkami poprzez zawarte w nich grupy amidowe.
6.8 Zachowanie fazowe
Izotropowe nieciągłe fazy sześcienne obserwuje się dla środków powierzchniowo czynnych w bardzo wysokich stężeniach.Cząsteczki surfaktantu o bardzo dużych grupach główek mają tendencję do tworzenia agregatów o mniejszej krzywiźnie dodatniej.markiz i in.zbadali zachowanie fazowe systemów 12Lys12/12Ser i 8Lys8/16Ser (patrz ryc. 10), a wyniki pokazały, że system 12Lys12/12Ser ma strefę separacji faz między obszarami roztworów micelarnych i pęcherzykowych, podczas gdy system 8Lys8/16Ser Układ 8Lys8/16Ser wykazuje ciągłe przejście (wydłużony obszar fazy micelarnej między obszarem małej fazy micelarnej a obszarem fazy pęcherzykowej).Należy zauważyć, że w obszarze pęcherzyków układu 12Lys12/12Ser pęcherzyki zawsze współistnieją z micelami, podczas gdy w obszarze pęcherzyków układu 8Lys8/16Ser występują tylko pęcherzyki.
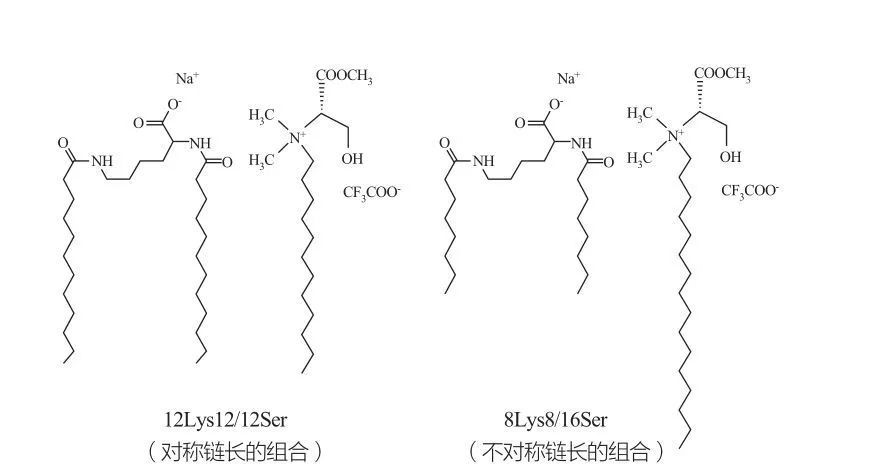
Mieszaniny kationowe surfaktantów na bazie lizyny i seryny: symetryczna para 12Lys12/12Ser (po lewej) i asymetryczna para 8Lys8/16Ser (po prawej)
6.9 Zdolność emulgująca
Kouchi i in.zbadali zdolność emulgowania, napięcie międzyfazowe, dyspergowalność i lepkość N-[3-dodecylo-2-hydroksypropylo]-L-argininy, L-glutaminianu i innych SAA.W porównaniu z syntetycznymi surfaktantami (ich konwencjonalnymi niejonowymi i amfoterycznymi odpowiednikami) wyniki wykazały, że AAS mają silniejsze zdolności emulgujące niż konwencjonalne surfaktanty.
Baczko i in.zsyntetyzowali nowe anionowe aminokwasowe środki powierzchniowo czynne i zbadali ich przydatność jako chiralnie zorientowanych rozpuszczalników do spektroskopii NMR.Szereg opartych na sulfonianach amfifilowych pochodnych L-Phe lub L-Ala z różnymi hydrofobowymi ogonami (pentylo-tetradecyl) zsyntetyzowano w reakcji aminokwasów z bezwodnikiem o-sulfobenzoesowym.Wu i in.zsyntetyzowane sole sodowe N-tłuszczowych acylo AAS izbadali ich zdolność emulgowania w emulsjach typu olej w wodzie, a wyniki wykazały, że te środki powierzchniowo czynne działały lepiej z octanem etylu jako fazą olejową niż z n-heksanem jako fazą olejową.
6.10 Postępy w syntezie i produkcji
Odporność na twardą wodę można rozumieć jako odporność środków powierzchniowo czynnych na obecność jonów, takich jak wapń i magnez, w twardej wodzie, tj. zdolność do unikania wytrącania się w mydłach wapniowych.Środki powierzchniowo czynne o wysokiej odporności na twardą wodę są bardzo przydatne w preparatach detergentowych i produktach higieny osobistej.Odporność na twardą wodę można ocenić, obliczając zmianę rozpuszczalności i aktywności powierzchniowej środka powierzchniowo czynnego w obecności jonów wapnia.
Innym sposobem oceny odporności na twardą wodę jest obliczenie procentu lub gramów środka powierzchniowo czynnego wymaganego do zdyspergowania w wodzie mydła wapniowego utworzonego ze 100 g oleinianu sodu.Na obszarach o wysokiej twardości wody wysokie stężenia jonów wapnia i magnezu oraz zawartość minerałów mogą utrudniać niektóre praktyczne zastosowania.Często jon sodu jest używany jako przeciwjon syntetycznego anionowego środka powierzchniowo czynnego.Ponieważ dwuwartościowy jon wapnia jest związany z obydwoma cząsteczkami środka powierzchniowo czynnego, powoduje on łatwiejsze wytrącanie się środka powierzchniowo czynnego z roztworu, co zmniejsza prawdopodobieństwo działania detergentowego.
Badanie odporności AAS na twardą wodę wykazało, że na odporność na kwasy i twardą wodę silny wpływ miała dodatkowa grupa karboksylowa, a odporność na kwasy i twardą wodę dalej wzrastała wraz ze wzrostem długości grupy oddzielającej między dwiema grupami karboksylowymi .Kolejność odporności na działanie kwasów i twardej wody była następująca: glicynian C12 < asparaginian C12 < glutaminian C12.Porównując odpowiednio dikarboksylowane wiązanie amidowe i dikarboksylowany surfaktant aminowy stwierdzono, że zakres pH tego drugiego był szerszy, a jego aktywność powierzchniowa wzrastała wraz z dodatkiem odpowiedniej ilości kwasu.Dikarboksylowane aminokwasy N-alkilowe wykazywały działanie chelatujące w obecności jonów wapnia, a asparaginian C12 tworzył biały żel.Glutaminian c 12 wykazywał dużą aktywność powierzchniową przy wysokim stężeniu Ca 2+ i oczekuje się, że znajdzie zastosowanie w odsalaniu wody morskiej.
6.11 Rozpraszalność
Dyspergowalność odnosi się do zdolności środka powierzchniowo czynnego do zapobiegania koalescencji i sedymentacji środka powierzchniowo czynnego w roztworze.Dyspergowalność jest ważną właściwością środków powierzchniowo czynnych, która sprawia, że nadają się one do stosowania w detergentach, kosmetykach i farmaceutykach.Środek dyspergujący musi zawierać wiązanie estrowe, eterowe, amidowe lub aminowe między grupą hydrofobową a końcową grupą hydrofilową (lub między prostołańcuchowymi grupami hydrofobowymi).
Ogólnie anionowe środki powierzchniowo czynne, takie jak siarczany alkanoloamidów i amfoteryczne środki powierzchniowo czynne, takie jak amidosulfobetaina, są szczególnie skuteczne jako środki dyspergujące mydła wapniowe.
Wiele wysiłków badawczych określiło dyspersyjność AAS, gdzie stwierdzono, że N-lauroilo-lizyna jest słabo kompatybilna z wodą i trudna w użyciu w preparatach kosmetycznych.W tej serii zasadowe aminokwasy podstawione N-acylem mają doskonałą dyspergowalność i są stosowane w przemyśle kosmetycznym do ulepszania receptur.
07 Toksyczność
Konwencjonalne środki powierzchniowo czynne, zwłaszcza kationowe środki powierzchniowo czynne, są wysoce toksyczne dla organizmów wodnych.Ich ostra toksyczność jest spowodowana zjawiskiem oddziaływania surfaktantów adsorpcyjno-jonowych na granicy faz komórka-woda.Zmniejszenie cmc surfaktantów zwykle prowadzi do silniejszej adsorpcji międzyfazowej surfaktantów, co zwykle skutkuje ich podwyższoną toksycznością ostrą.Zwiększenie długości łańcucha hydrofobowego środków powierzchniowo czynnych prowadzi również do wzrostu ostrej toksyczności środka powierzchniowo czynnego.Większość SAA jest mało toksyczna lub nietoksyczna dla ludzi i środowiska (szczególnie dla organizmów morskich) i nadaje się do stosowania jako składniki żywności, farmaceutyki i kosmetyki.Wielu badaczy wykazało, że surfaktanty aminokwasowe są delikatne i niedrażniące dla skóry.Wiadomo, że środki powierzchniowo czynne na bazie argininy są mniej toksyczne niż ich konwencjonalne odpowiedniki.
Brito i in.badał właściwości fizykochemiczne i toksykologiczne aminokwasów amfifilowych i ich [pochodnych tyrozyny (Tyr), hydroksyproliny (Hyp), seryny (Ser) i lizyny (Lys)] spontanicznego tworzenia pęcherzyków kationowych i podał dane dotyczące ich ostrej toksyczności dla Daphnia magna (IC 50).Zsyntetyzowali pęcherzyki kationowe bromku dodecylotrimetyloamoniowego (DTAB)/pochodnych Lys i/lub mieszanin pochodnych Ser/Lys i przetestowali ich ekotoksyczność i potencjał hemolityczny, wykazując, że wszystkie SAA i ich mieszaniny zawierające pęcherzyki były mniej toksyczne niż konwencjonalny środek powierzchniowo czynny DTAB .
Rosa i in.badali wiązanie (asocjację) DNA ze stabilnymi pęcherzykami kationowymi na bazie aminokwasów.W przeciwieństwie do konwencjonalnych kationowych środków powierzchniowo czynnych, które często wydają się być toksyczne, oddziaływanie kationowych aminokwasowych środków powierzchniowo czynnych wydaje się być nietoksyczne.Kationowy SAA oparty jest na argininie, która spontanicznie tworzy stabilne pęcherzyki w połączeniu z niektórymi anionowymi środkami powierzchniowo czynnymi.Inhibitory korozji na bazie aminokwasów również są uważane za nietoksyczne.Te środki powierzchniowo czynne są łatwo syntetyzowane z wysoką czystością (do 99%), niskim kosztem, łatwo biodegradowalnymi i całkowicie rozpuszczalnymi w środowisku wodnym.Kilka badań wykazało, że środki powierzchniowo czynne zawierające aminokwasy siarkowe są lepsze w hamowaniu korozji.
W niedawnym badaniu Perinelli i in.opisali zadowalający profil toksykologiczny ramnolipidów w porównaniu z konwencjonalnymi środkami powierzchniowo czynnymi.Wiadomo, że ramnolipidy działają jako środki zwiększające przepuszczalność.Opisali również wpływ ramnolipidów na przepuszczalność nabłonka leków wielkocząsteczkowych.
08 Działanie przeciwdrobnoustrojowe
Działanie przeciwdrobnoustrojowe środków powierzchniowo czynnych można ocenić na podstawie minimalnego stężenia hamującego.Szczegółowo zbadano działanie przeciwdrobnoustrojowe środków powierzchniowo czynnych na bazie argininy.Stwierdzono, że bakterie Gram-ujemne są bardziej odporne na środki powierzchniowo czynne na bazie argininy niż bakterie Gram-dodatnie.Aktywność przeciwbakteryjna środków powierzchniowo czynnych jest zwykle zwiększona przez obecność wiązań hydroksylowych, cyklopropanowych lub nienasyconych w łańcuchach acylowych.Castillo i in.wykazali, że długość łańcuchów acylowych i ładunek dodatni określają wartość HLB (równowaga hydrofilowo-lipofilowa) cząsteczki, a te mają wpływ na ich zdolność do rozrywania błon.Ester metylowy Nα-acylargininy jest inną ważną klasą kationowych środków powierzchniowo czynnych o szerokim spektrum aktywności przeciwbakteryjnej i łatwo ulega biodegradacji i ma niską toksyczność lub nie ma jej wcale.Badania interakcji surfaktantów na bazie estrów metylowych Nα-acylargininy z 1,2-dipalmitoilo-sn-propylotrioksylo-3-fosforylocholiną i 1,2-ditetradekanoilo-sn-propylotrioksylo-3-fosforylocholiną, membranami modelowymi oraz z żywymi organizmami w obecność lub nieobecność barier zewnętrznych wykazała, że ta klasa środków powierzchniowo czynnych ma dobre działanie przeciwdrobnoustrojowe. Wyniki wykazały, że środki powierzchniowo czynne mają dobrą aktywność przeciwbakteryjną.
09 Właściwości reologiczne
Właściwości reologiczne surfaktantów odgrywają bardzo ważną rolę w określaniu i przewidywaniu ich zastosowań w różnych gałęziach przemysłu, w tym w przemyśle spożywczym, farmaceutycznym, wydobywczym ropy naftowej, produktach higieny osobistej i chemii gospodarczej.Przeprowadzono wiele badań w celu omówienia związku między lepkosprężystością surfaktantów aminokwasowych a cmc.
10 Zastosowania w przemyśle kosmetycznym
AAS są wykorzystywane w formułowaniu wielu produktów higieny osobistej.Stwierdzono, że glicynian N-kokoilu potasu jest łagodny dla skóry i jest stosowany do oczyszczania twarzy w celu usunięcia szlamu i makijażu.Kwas n-acylo-L-glutaminowy ma dwie grupy karboksylowe, dzięki czemu jest lepiej rozpuszczalny w wodzie.Wśród tych AAS, AAS oparte na kwasach tłuszczowych C12 są szeroko stosowane w oczyszczaniu twarzy w celu usunięcia szlamu i makijażu.AAS z łańcuchem C18 są stosowane jako emulgatory w produktach do pielęgnacji skóry, a sole N-lauryloalaniny są znane z tworzenia kremowych pianek, które nie podrażniają skóry i dlatego mogą być stosowane w formułowaniu produktów do pielęgnacji niemowląt.AAS na bazie N-laurylu stosowane w pastach do zębów mają dobre właściwości myjące podobne do mydła i silne działanie hamujące enzymy.
W ciągu ostatnich kilkudziesięciu lat wybór środków powierzchniowo czynnych do kosmetyków, środków higieny osobistej i farmaceutyków koncentrował się na niskiej toksyczności, łagodności, delikatności w dotyku i bezpieczeństwie.Konsumenci tych produktów są w pełni świadomi potencjalnego podrażnienia, toksyczności i czynników środowiskowych.
Obecnie AAS są używane do formułowania wielu szamponów, farb do włosów i mydeł do kąpieli ze względu na ich liczne zalety w porównaniu z ich tradycyjnymi odpowiednikami w kosmetykach i produktach higieny osobistej.Surfaktanty na bazie białek posiadają pożądane właściwości niezbędne w produktach higieny osobistej.Niektóre AAS mają zdolność tworzenia filmu, podczas gdy inne mają dobre właściwości pienienia.
Aminokwasy są ważnymi naturalnie występującymi czynnikami nawilżającymi w warstwie rogowej naskórka.Kiedy komórki naskórka obumierają, stają się częścią warstwy rogowej naskórka, a białka wewnątrzkomórkowe są stopniowo rozkładane do aminokwasów.Aminokwasy te są następnie transportowane dalej do warstwy rogowej naskórka, gdzie wchłaniają tłuszcz lub substancje tłuszczopodobne do warstwy rogowej naskórka, poprawiając w ten sposób elastyczność powierzchni skóry.Około 50% naturalnego czynnika nawilżającego w skórze składa się z aminokwasów i pirolidonu.
Kolagen, powszechny składnik kosmetyków, zawiera również aminokwasy, które zapewniają skórze miękkość.Problemy ze skórą, takie jak szorstkość i matowość, są w dużej mierze spowodowane brakiem aminokwasów.Jedno z badań wykazało, że zmieszanie aminokwasu z maścią łagodzi oparzenia skóry, a dotknięte obszary wracają do normalnego stanu bez bliznowców.
Stwierdzono również, że aminokwasy są bardzo przydatne w pielęgnacji uszkodzonych skórek.Suche, pozbawione kształtu włosy mogą wskazywać na spadek stężenia aminokwasów w mocno zniszczonej warstwie rogowej naskórka.Aminokwasy mają zdolność penetracji łusek do łodygi włosa i wchłaniania wilgoci ze skóry.Ta zdolność środków powierzchniowo czynnych na bazie aminokwasów czyni je bardzo przydatnymi w szamponach, farbach do włosów, zmiękczaczach do włosów, odżywkach do włosów, a obecność aminokwasów wzmacnia włosy.
11 Zastosowania w kosmetyce codziennej
Obecnie na całym świecie rośnie zapotrzebowanie na preparaty detergentowe na bazie aminokwasów.Wiadomo, że AAS mają lepsze właściwości czyszczące, pienne i zmiękczające tkaniny, co czyni je odpowiednimi do domowych detergentów, szamponów, płynów do mycia ciała i innych zastosowań.Podano, że amfoteryczny AAS pochodzący z kwasu asparaginowego jest wysoce skutecznym detergentem o właściwościach chelatujących.Stwierdzono, że stosowanie składników detergentów składających się z N-alkilo-β-aminoetoksykwasów zmniejsza podrażnienia skóry.Opisano, że płynny preparat detergentowy składający się z N-kokoilo-β-aminopropionianu jest skutecznym detergentem do usuwania plam olejowych na powierzchniach metalowych.Wykazano również, że środek powierzchniowo czynny będący kwasem aminokarboksylowym, C 14 CHOHCH 2 NHCH 2 COONa, ma lepsze właściwości czyszczące i jest stosowany do czyszczenia tekstyliów, dywanów, włosów, szkła itp. Kwas 2-hydroksy-3-aminopropionowy-N,N- Wiadomo, że pochodna kwasu acetylooctowego ma dobrą zdolność kompleksowania, a tym samym nadaje stabilność środkom wybielającym.
Przygotowanie preparatów detergentowych na bazie N-(N'-długołańcuchowej acylo-β-alanylo)-β-alaniny zostało opisane przez Keigo i Tatsuya w ich patencie na lepszą zdolność i stabilność prania, łatwe rozbijanie piany i dobre zmiękczanie tkanin .Firma Kao opracowała formułę detergentu opartą na N-acylo-1-N-hydroksy-β-alaninie i odnotowała niskie podrażnienia skóry, wysoką odporność na wodę i wysoką skuteczność usuwania plam.
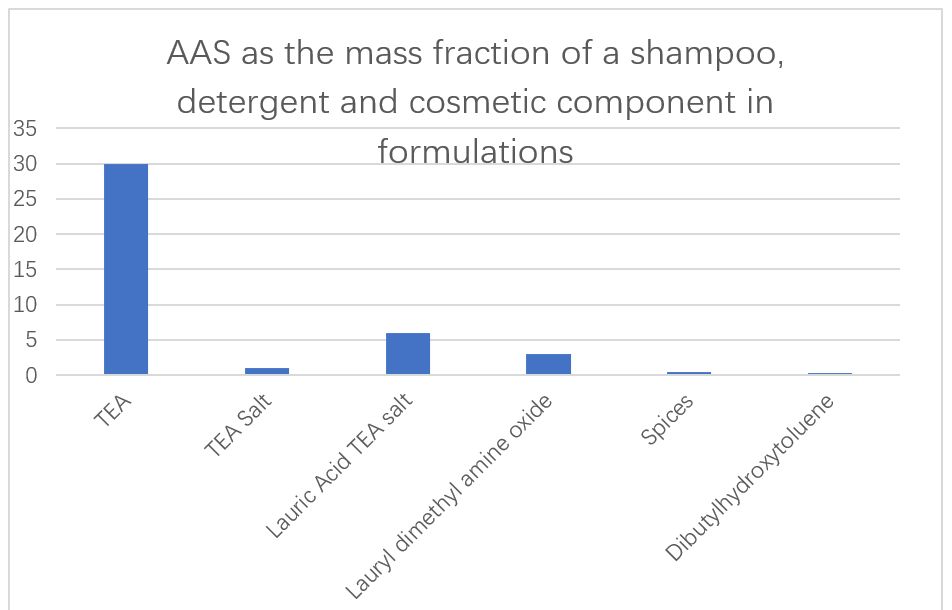
Japońska firma Ajinomoto wykorzystuje niskotoksyczne i łatwo degradowalne SAA na bazie kwasu L-glutaminowego, L-argininy i L-lizyny jako główne składniki szamponów, detergentów i kosmetyków (ryc. 13).Opisano również zdolność dodatków enzymatycznych w preparatach detergentowych do usuwania zanieczyszczeń białkowych.N-acylo AAS pochodzące z kwasu glutaminowego, alaniny, metyloglicyny, seryny i kwasu asparaginowego opisano jako doskonałe ciekłe detergenty w roztworach wodnych.Te środki powierzchniowo czynne w ogóle nie zwiększają lepkości, nawet w bardzo niskich temperaturach, i można je łatwo przenosić ze zbiornika magazynowego urządzenia do spieniania w celu uzyskania jednorodnych pianek.
Czas postu: 09-06-2022

